Варианты генов, ассоциированные с лейкемией, могут продуцировать "неправильные" иммунные клетки, которые приводят к развитию аутоиммунных заболеваний, говорится в новом исследовании.
Ранее ученые заметили, что у пациентов с лейкемией также вероятно развитие аутоиммунных заболеваний, таких как ревматоидный артрит или апластическая анемия. Изучение этой связи показало, что ключевую роль играют Т-киллеры. Новое исследование позволяет понять, какую роль играют Т-киллеры в развитии лейкемии и аутоиммунных заболеваний. Вариации генов, влияющие на белок, который контролирует рост Т-киллеров, могут превратить их в изгоев, обнаружили исследователи.
"Мы показали, что эти неконтролируемые Т-киллеры являются движущей силой аутоиммунитета. Они, вероятно, являются одним из типов клеток, непосредственно способствующих развитию аутоиммунного заболевания", - рассказал соавтор статьи, опубликованной в журнале Immunity Этьен Масл-Фаркхар, исследователь в лаборатории иммуногеномики и геномной медицины Института медицинских исследований Гарвана.
"Наше исследование также сужает круг путей, которые могут быть полезны при нацеливании на эти клетки для будущего лечения. Мы знали, что люди с различными аутоиммунными заболеваниями со временем приобретают эти неконтролируемые клетки-киллеры, а также то, что воспаление может привести к размножению иммунных клеток и развитию мутаций. Мы поставили перед собой задачу выяснить, вызывают ли неконтролируемые Т-клетки эти аутоиммунные заболевания или просто ассоциируются с ними", - сообщил он.
Исследователи использовали новые методы скрининга с высоким разрешением для изучения образцов крови детей с редкими наследственными аутоиммунными заболеваниями. Затем они применили метод CRISPR/Cas9, инструмент редактирования генома, в мышиных моделях, чтобы выяснить, что происходит при генетическом изменении белка STAT3. STAT3 встречается во всем организме и имеет решающее значение для различных клеточных функций, включая контроль над B- и T-клетками иммунной системы.
Исследователи обнаружили, что если эти белки изменены, они могут вызвать бесконтрольный рост неконтролируемых клеток-киллеров, что приводит к увеличению клеток, которые в обход иммунных контрольных точек атакуют собственные клетки организма. При этом даже 1-2% неконтролируемых Т-клеток человека могут вызвать аутоиммунное заболевание.
"Никогда не было ясно, какова связь между лейкемией и аутоиммунными заболеваниями - является ли измененный белок STAT3 причиной болезни, или лейкемические клетки делятся и приобретают эту мутацию просто как побочный продукт. Это настоящий вопрос курицы и яйца, который удалось решить благодаря работе Масл-Фаркхара", - комментирует профессор Крис Гудноу, руководитель лаборатории иммуногеномики Института Гарвана. "Это дает несколько действительно хороших шансов на то, что мы сможем сделать лучше в плане борьбы с этими заболеваниями, которые угрожают жизни", - добавил он.
Будущее применение может включать более точное нацеливание медикаментов, таких как уже одобренные ингибиторы JAK, на основе наличия этих мутаций. "Теперь мы можем искать Т-клетки с вариациями STAT3. Это большой шаг вперед в определении того, кто является плохим парнем", - утверждает профессор Гудноу.
Исследование также выявило две специфические рецепторные системы, которые связаны со стрессом. "Частично то, что заставляет эти клетки-изгои становиться киллерами, связано со стресс-сенсорными путями. Существует много взаимосвязей между стрессом, повреждениями и старением. Теперь у нас есть убедительные доказательства того, как это связано с аутоиммунитетом", - отмечает Гудноу.
Исследование ученых может помочь в разработке технологии скрининга, которую клиницисты смогут использовать для последовательного анализа полного генома каждой клетки в образце крови, чтобы определить, какие клетки могут стать неконтролируемыми и вызвать заболевание. Необходимы дальнейшие исследования, чтобы определить, вовлечены ли Т-киллеры во все аутоиммунные заболевания, и какая доля людей с ревматоидным артритом и другими аутоиммунными заболеваниями имеют эти клетки и вариации STAT3.
Masle-Farquhar, E., et al. Мутации усиления функции STAT3 связывают лейкемию с аутоиммунным заболеванием путем патологической дисрегуляции и накопления CD8+ Т-клеток NKG2Dhi (аннотация).
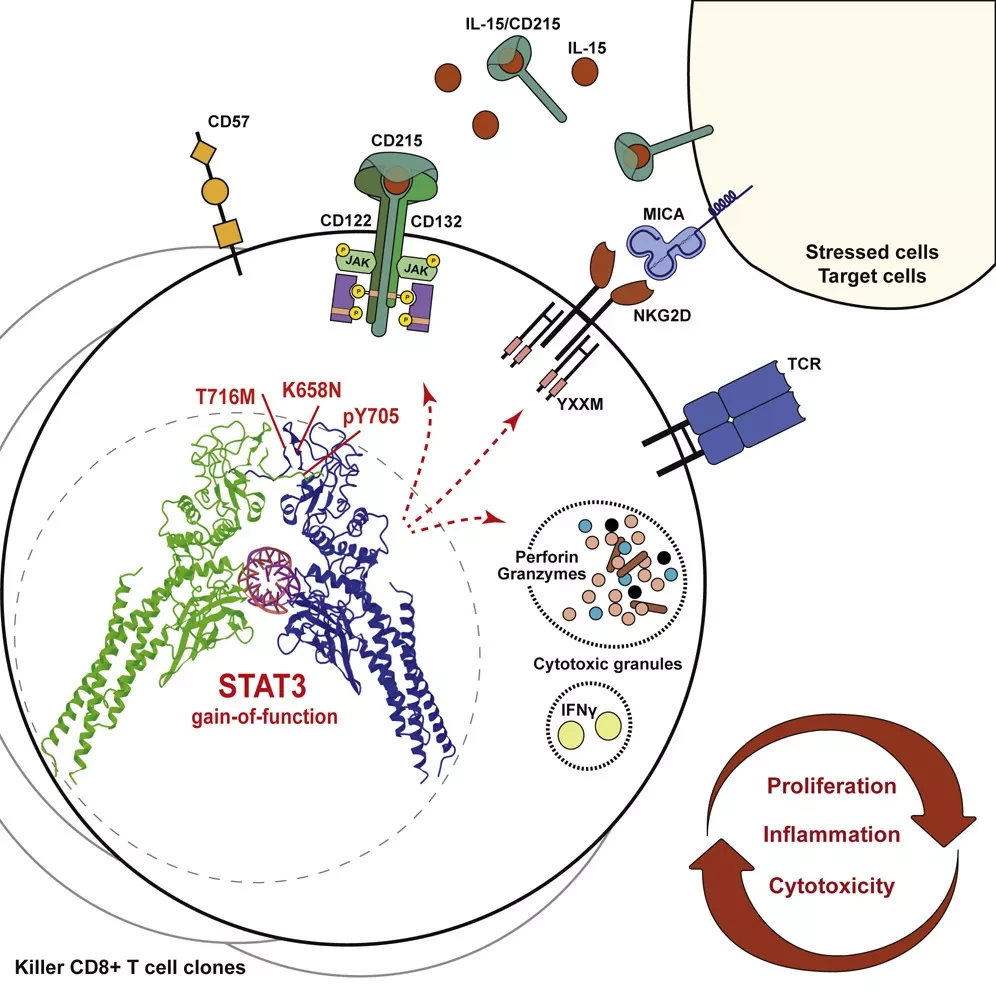
Ассоциация между раком и аутоиммунным заболеванием остается необъяснимой, примером чего может служить Т-клеточный крупноклеточный гранулярный лимфоцитарный лейкоз (T-LGL), при котором соматические мутации STAT3 с усилением функции (GOF) коррелируют с сопутствующим аутоиммунитетом.
Чтобы выяснить, являются ли эти мутации причиной или следствием клональной экспансии CD8+ Т-клеток и аутоиммунитета, мы проанализировали пациентов и мышей с герминальными GOF-мутациями STAT3. Мутации STAT3 GOF способствовали накоплению эффекторных клонов CD8+ Т-клеток, высоко экспрессирующих NKG2D, рецептор для молекул MHC-класса-I, ассоциированных со стрессом. Это подмножество также экспрессировало гены гранзимов, перфорина, интерферона-γ и Ccl5/Rantes и требовало NKG2D и рецептора IL-15/IL-2 IL2RB для максимального накопления. Ограниченный лейкоцитами STAT3 GOF был достаточным, а CD8+ Т-клетки были необходимы для летальной патологии у мышей.
Эти результаты показывают, что мутации STAT3 GOF вызывают эффекторное накопление олигоклональных CD8+ Т-клеток и что эти клетки-изгои способствуют аутоиммунной патологии, поддерживая гипотезу о том, что соматические мутации в драйверных генах лейкемии/лимфомы способствуют развитию аутоиммунного заболевания.