Ирландские и немецкие ученые определили, как специфические иммунные клетки могут работать вместе в жировой ткани, вызывая воспаление, которое приводит к увеличению веса и ожирению.
Их работа открывает новые пути для использования регулирования этого воспаления в жировой ткани, тем самым предлагая новые способы борьбы с ожирением.
Существует глобальная эпидемия ожирения среди взрослых и детей, причем люди с ожирением предрасположены к развитию диабета, сердечно-сосудистых заболеваний и рака. Для решения этой проблемы необходимы новые методы лечения. В своем исследовании ученые определили, как "белки контрольных точек" и иммунные клетки изменяют воспалительные клетки в жировой ткани, вызывая ожирение. У людей с ожирением (индекс массы тела BMI> 30 кг/м²) изменения в экспрессии чекпойнтов в висцеральном жире предсказывали вес человека. Затем ученые показали, что изменения в так называемых белках иммунных контрольных точек у мышей, сидящих на "высокожировой" диете, связаны с резким снижением развития ожирения и диабета.
Исследование, только что опубликованное в ведущем международном биомедицинском журнале Science Translational Medicine, проводилось под руководством профессора Падраика Фаллона из медицинской школы Тринити-колледжа в Дублине. Профессор Фаллон прокомментировал: "Этот новый процесс регуляции контрольных точек клеток в висцеральной жировой ткани людей, страдающих ожирением, продвигает наше понимание того, как иммунная система контролирует вызванное диетой увеличение веса, которое может привести к таким заболеваниям, как ожирение и диабет 2 типа".
"Наше открытие имеет более широкое значение для решения вопроса о том, как ожирение влияет на сопутствующие заболевания, как это было видно на примере пандемии COVID-19, когда у людей с ожирением, инфицированных SARS-CoV-2, чаще развивается тяжелая форма заболевания, требующая интенсивной терапии, а также повышается риск летального исхода".
"В нашем исследовании мы проанализировали функцию иммунных контрольных точек на конкретных клетках, и очень интересно видеть, что небольшое изменение в одной из многих популяций клеток в жировой ткани оказывает такое влияние на исход заболевания. Только благодаря нашим фундаментальным исследованиям с использованием доклинических моделей мы смогли получить доступ к образцам пациентов и связать наши выводы с заболеваниями человека. Теперь будет интересно изучить, как мы можем манипулировать этими контрольными точками на конкретных популяциях клеток, представляющих интерес, чтобы помочь людям с ожирением".
Christian Schwartz et al. Врожденный PD-L1 ограничивает Т-клеточно-опосредованное воспаление жировой ткани и смягчает вызванное диетой ожирение (аннотация).
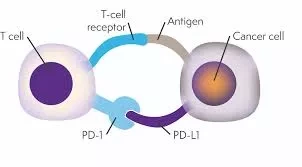
Ожирение стало одной из основных проблем здравоохранения в промышленно развитом мире. Иммунная регуляция играет важную роль в гомеостазе жировой ткани, однако начальные события, которые смещают баланс от невоспалительной гомеостатической среды к воспалению, приводящему к ожирению, мало изучены. В данном отчете мы сообщаем о роли ко-стимулирующей молекулы программируемой смерти-лиганда 1 (PD-L1) в ограничении ожирения, вызванного диетой. Функциональная абляция PD-L1 на дендритных клетках (ДК) с помощью условно нокаутных мышей увеличивала набор веса и метаболический синдром при ожирении, вызванном диетой, тогда как экспрессия PD-L1 на врожденных лимфоидных клетках второго типа (ILC2s), Т-клетках и макрофагах не требовала контроля ожирения.
Используя кокультуры in vitro, ДК взаимодействовали с Т-клетками и ILC2 через ось PD-L1:PD-1, подавляя пролиферацию Т-хелперов типа 1 и способствуя поляризации типа 2, соответственно. Роль PD-L1 в регуляции жировой ткани была также показана на людях, с положительной корреляцией между экспрессией PD-L1 в висцеральном жире людей с ожирением и повышенной массой тела.
Таким образом, мы определили механизм гомеостаза жировой ткани, контролируемый экспрессией PD-L1 ДК, что может быть клинически значимой находкой в отношении связанных с иммунитетом побочных явлений во время терапии ингибиторами иммунных чекпойнтов.