Новый диагностический метод, позволяющий предсказать, будет ли онкологический пациент реагировать на иммунотерапию, был разработан учеными University of Bath.
Одним из видов иммунотерапии, называемым терапией чекпойнт ингибиторами, представляет собой антитела, которые отпускают тормоза, которые опухоль наложила на иммунную систему. Это активизирует естественную противораковую реакцию, которая затем уничтожает опухоль.
В то время как у некоторых пациентов иммунотерапия с использованием чекпойнт ингибиторов очень успешна, у других она малоэффективна или вообще не оказывает никакого эффекта. Учитывая риски токсичности, присущие таким методам лечения, растет необходимость определения того, какие пациенты могут получить наибольшую пользу, избегая ненужного воздействия на тех, кому это не поможет.
Исследователи Банафше Лариджани (Banafshé Larijani), директора Центра терапевтических инноваций (CTI-Bath), в сотрудничестве с другими коллегами и компанией FASTBASE Solutions Ltd., в настоящее время разработали метод прогнозирования на основе продвинутой платформы микроскопирования, который определяет взаимодействие иммунных клеток с опухолевыми клетками, а также сообщает о состоянии активации иммунных чекпойнтов, которые ослабляют противоопухолевую реакцию.
Группа опубликовала свои результаты в журнале "Cancer Research" ("Исследование рака") Американской ассоциации по изучению рака.
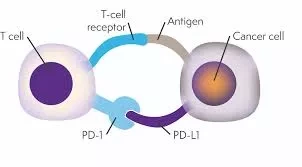
Изучался иммунный чекпойнт, состоящий из двух белков, называемых PD-1 (присутствующих на Т-лимфоцитах) и PD-L1 (присутствующих на других типах иммунных клеток и на поверхности многих различных типов опухолей).
Обычно, когда PD-1 на поверхности Т-лимфоцитов вступает в контакт с PD-L1 на поверхности других иммунных клеток, это эффективно отключает иммунную функцию Т-клетки. У здоровых людей эти чекпойнт (контрольно-пропускные пункты) жестко регулируют иммунный ответ организма, действуя как отключающее устройство для предотвращения аутоиммунных и воспалительных заболеваний.
Опухолевые клетки, по сути, блокируют этот механизм, экспрессируя PD-L1 на своей поверхности, что позволяет им активировать PD-1 на Т-лимфоците, тем самым отключая его противоопухолевую функцию, обеспечивая выживание и рост опухоли.
Ингибиторы чекпойнт иммунотерапии работают, нарушая взаимодействие между PD-L1 на опухоли и PD-1 на Т-лимфоците, и таким образом восстанавливают противоопухолевую активность.
Новый метод определяет степень взаимодействия PD-1/PD-L1 при биопсии опухоли, предсказывая, будет ли терапия ингибиторами чекпойнт иметь значительное клиническое преимущество. Новаторские результаты показывают, что у пациентов, проходящих иммунотерапию (метастатического немелкоклеточного рака легкого) с низкой степенью взаимодействия PD-1/PD-L1, результат лечения значительно хуже, чем у пациентов с высоким уровнем взаимодействия.
Профессор Лариджани объяснил: "В настоящее время решения о том, следует ли продолжать лечение с помощью ингибиторов чекпойнт, основываются просто на том, присутствуют ли PD-1 и PD-L1 в биопсии, а не на их функциональном состоянии. Однако наша работа показала, что гораздо важнее знать, что эти два белка на самом деле взаимодействуют и, следовательно, могут оказывать функциональное воздействие на выживаемость опухоли".
Профессор Хосе И Лопес (José I López) кафедры патологии Университетской больницы Крусеса (Бильбао, Испания) и соавтор этого исследования, сказал: "Иммунная блокада чекпойнт становится теперь терапевтической вехой в борьбе с некоторыми видами рака".
"Пациенты выбираются для этого варианта лечения с использованием иммуногистохимии, однако, эта техника не позволяет надежно выявить всех кандидатов, которые потенциально могли бы быть излечены. На самом деле, есть до 19% пациентов, которые предположительно отрицательно реагируют на эту терапию".
Профессор Стивен Уорд, заместитель председателя CTI-Bath и соавтор исследования: "Инструмент, который мы разработали, является важным шагом на пути к персонализированной медицине". Используя его, мы можем точно определить, кто получит пользу от иммунотерапии".
Он также покажет, какие пациенты вряд ли будут реагировать задолго до того, как начнут длительный курс лечения, и этим пациентам можно будет предложить другой путь лечения".
Следующие шаги заключаются во внедрении этой платформы визуализации в национальные и международные испытания для оценки того, как этот инструмент прогнозирования может быть использован в качестве сопутствующего диагностического средства.