Исследование, опубликованное в журнале Cell Reports, раскрывает важные аспекты молекулярных механизмов, которые лежат в основе естественной защиты организма от развития рака кожи.
Результаты этой работы дают новые сведения о поведении рака кожи на клеточном уровне и открывают путь к новым потенциальным терапевтическим мишеням для лечения этого заболевания.
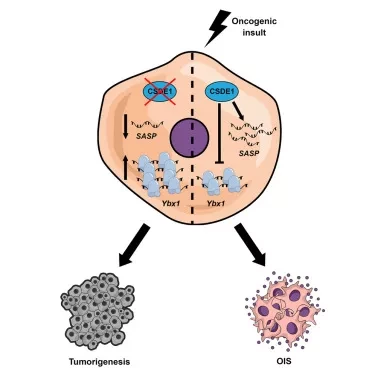
"Мы обнаружили, что белок CSDE1 координирует сложную цепь событий, которые обеспечивают старение клеток кожи, значительно замедляя их функционирование и не приводя к их отмиранию", - говорит Розарио Аволио, первый автор исследования. "Образовавшиеся клетки действуют как брандмауэр против рака, подавляя образование опухолей".
Исследователи из Центра геномного регулирования (CRG) провели исследование, отобрав у мышей кератиноциты - наиболее распространенный тип клеток эпидермиса кожи. Кератиноциты могут давать начало различным типам рака кожи, включая базальную и сквамозную клеточные карциномы, две наиболее часто встречающиеся формы всех видов рака человека. Группа экспериментально ввела гены, способствующие развитию рака, что привело клетки в состояние старения. Они обнаружили, что когда уровень CSDE1 был снижен, клетки не поддавались старению и приобретали способность к бессмертию, что является необходимым этапом в развитии рака.
Дальнейшие эксперименты показали, что когда клетки, лишенные CSDE1, были имплантированы под кожу мышей, они начали образовывать злокачественные опухоли. Авторы сочли это поразительным, поскольку у каждой из обработанных мышей в течение 15-20 дней развивалась плоскоклеточная карцинома, что подчеркивает важность CSDE1 в подавлении опухолей.
Исследователи обнаружили, что CSDE1 способствует подавлению опухоли с помощью двух различных механизмов. CSDE1 побуждает клетку выделять коктейль цитокинов и ферментов, которые заставляют клетку входить в состояние перманентной остановки роста. CSDE1 также останавливает синтез YBX1, белка, который, как ранее было известно, способствует росту и агрессивности опухоли.
По словам авторов, результаты исследования важны, так как ранее считалось, что CSDE1 способствует образованию раковых опухолей, а не подавляет их. Предыдущие исследования той же группы показали, что CSDE1 способствует образованию метастазов меланомы, менее распространенном, но наиболее агрессивном типе рака кожи. Другие работы показали, что CSDE1 связан с пролиферацией опухоли при многих видах рака.
"CSDE1 - это в большой степени "доктор Джекил и мистер Хайд" среди белков. Он обладает непредсказуемой двойственной природой в зависимости от типа клеток и тканей", - объясняет Аволио.
"Мы не знаем, почему этот белок вызывает рак в одних случаях и подавляет его в других. Изучение первопричины этого будет иметь важные последствия для открытия новых, более персонализированных методов лечения рака".
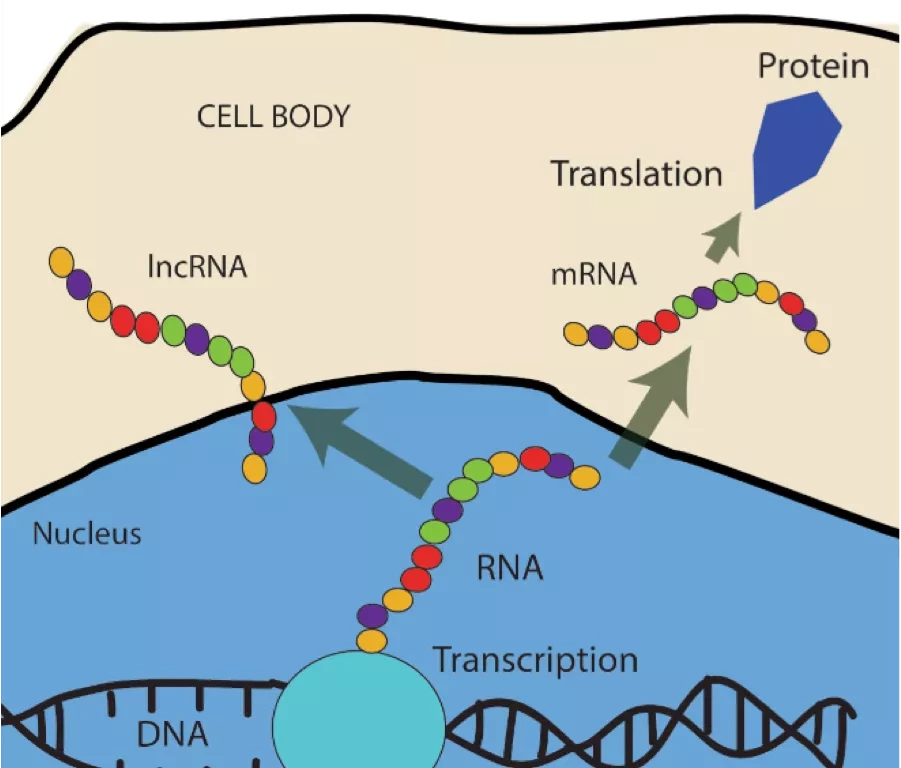
CSDE1 - это РНК-связывающий белок, тип белка, который контролирует РНК, часто сразу после их создания с возможностью значительного изменения их функции. Одна из возможных теорий, объясняющих, почему CSDE1 ведет себя по-разному, заключается в том, что нормальные клетки кожи и клетки опухоли имеют немного разные варианты белка, которые по-разному влияют на более общий молекулярный механизм.
Это исследование - одно из немногих, в котором изучается роль РНК-связывающих белков в формировании клеточного старения, что является новым важным направлением в исследовании рака. "Долгое время считалось, что РНК-связывающие белки - это универсальные молекулы, которые клетки используют для общего поддержания жизнедеятельности, и что на них нельзя воздействовать терапевтически. Становится все более очевидным, что это не так, и что эта новая область имеет решающее значение для понимания заболеваний человека", - заключает Аволио.
Rosario Avolio et al. Скоординированный посттранскрипционный контроль онкоген-индуцированного старения с помощью UNR/CSDE1 (аннотация).
Онкоген-индуцированное старение (OIS ) - это форма стабильной остановки клеточного цикла, возникающая в ответ на онкогенную стимуляцию. Для трансформации необходимо обойти OIS, но механизмы формирования и обхода OIS остаются малоизученными, особенно на посттранскрипционном уровне.
В данном исследовании мы показали, что РНК-связывающий белок UNR/CSDE1 обеспечивает OIS в первичных кератиноцитах мыши. Истощение CSDE1 приводит к преодолению старения, иммортализации клеток и образованию опухолей, что указывает на то, что CSDE1 ведет себя как опухолевый супрессор. Непредвзятый высокопроизводительный анализ показал, что CSDE1 способствует OIS двумя независимыми молекулярными механизмами: повышением стабильности мРНК фактора Senescence-associated secretory phenotype (SASP) и репрессией трансляции мРНК Ybx1. Важно отметить, что истощение YBX1 из иммортальных кератиноцитов восстанавливает старение и устраняет остановку пролиферации из-за SASP, выявляя многоуровневые механизмы, используемые CSDE1 для координации старения.
Наши данные подчеркивают важность посттранскрипционного контроля в регуляции старения.