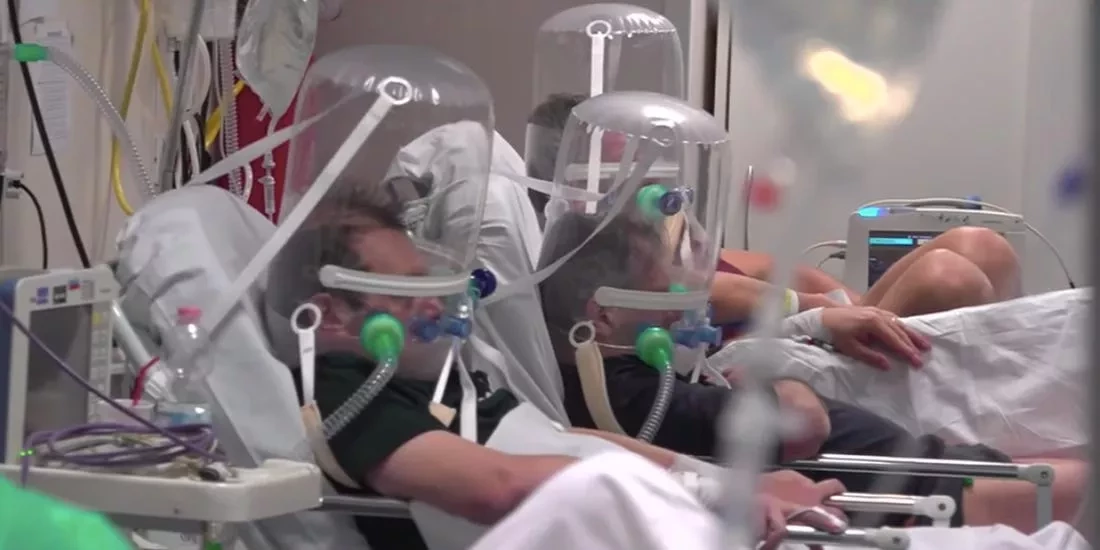
Пациенты с SARS-CoV-2 инфекцией склонны к тромботическим осложнениям, связанным с повышенной смертностью. Диспергированная внутрисосудистая коагуляция и тромботическая микроангиопатия являются важными патогенетическими факторами, однако их детальная патофизиология не выяснена в полной мере. Микрочастицы (МЧ) представляют собой небольшие фосфолипидные везикулы, происходящие обычно из различных клеток, таких как лейкоциты и эндотелиальные клетки, но в основном из тромбоцитов, играющих важную роль в свертывании крови и воспалении путем экспрессии прокоагулянтной активности.
Мы проспективно изучили 19 пациентов, госпитализированных в университетской клинике Патраса с 3 марта по 3 мая 2020 г., у которых по установленным критериям был диагностирован диагноз пневмония КОВИД-19. Кровь брали в течение 24 часов после госпитализации, перед терапией антикоагулянтами. Классификация тяжести пневмонии основывалась на рекомендациях Американского торакального общества. Профилактический низкомолекулярный гепарин (НМГ) назначался в соответствии с рекомендациями по лечению КОВИД-19. Препарат назначали пациентам с тяжелой респираторной недостаточностью (ТРН) на ИВЛ в течение 14 дней. Пациентам с ТРН проводили компьютерную томографическую ангиографию легких (КТЛА) для исключения тромбоэмболии. В контрольную группу были включены 19 здоровых людей.
Проводился полный анализ крови, биохимический профиль, С-реактивный белок, ферритин и факторы коагуляции. Антитромбин III (ATIII), S белок S (PS) и прокоагулятные фосфолипиды (PPL) измерялись на приборе STA-R (Diagnostica Stago) и с использованием реагентов того же производителя. Анализ активности ATIII и PS проводился методом хромогенных субстратов. PS анализировали клоттинг-методом. Активность PS измерялась с помощью теста STA Procoag-PPL. Сокращение времени образования сгустка указывало на увеличение PPL. Данные анализировались с помощью непараметрического теста Манна-Уитни.
Все обследуемые показали нормальные уровни природных ингибиторов коагуляции ATIII, PC и PS. По сравнению с контрольной группой у пациентов с КОВИД-19 пневмонией наблюдалось значительное увеличение PT, Д-димеров и фибриногена (p<0.001, соответственно) и значительное снижение времени свёртывания STA-procoag-PPL (p<0.001), что свидетельствует о более высокой активности PPL. Различия в активности PPL между пациентами с тяжелой (n=6) и не тяжелой (n=13) пневмонией у пациентов с КОВИД-19 отсутствовали. Пациенты с ТРН с потребностью в ИВЛ показали значительно более высокие уровни активности PPL при поступлении (p=0,045) и более высокие значения ферритина (p=0,038). Время свертывания STA-procoag-PPL положительно коррелировало с уровнями D-димеров и фибриногена (p<0,05, соответственно). В нашей исследуемой когорте при госпитализации не наблюдалось явных клинических или КТЛА-обнаруженных тромботических явлений.
У наших пациентов повышенный уровень D-димеров не сопровождались тромбоцитопенией или низким уровнем фибриногена. Важным результатом настоящего исследования является обнаружение повышенной активности PPL у пациентов с КОВИД-19 пневмонией при поступлении, независимо от тяжести пневмонии. Кроме того, более высокая активность PPL при поступлении была связана с прогрессированием КОВИД-19 пневмонии в ТРН. Следовательно, согласно представленным результатам, активность PPL, измеренная при госпитализации пациентов с КОВИД-19 пневмонией, не является индексом тяжести пневмонии, но может играть прогностическую роль для прогрессирования в ТРН. МЧ играют важную патофизиологическую роль в коагуляции и воспалении. Что касается роли PPL в воспалении, то более высокая активность PPL и ферритина при поступлении ассоциировалась с прогрессированием КОВИД-19 пневмонии в ТРН. Кроме того, у всех больных КОВИД-19 пневмонией активность PPL коррелировала с воспалительными показателями D-димеров и фибриногена. Несмотря на потенциальную протромботическую роль PPL, явных клинических или КТЛА-обнаруженных тромботических событий не наблюдалось, вероятнее всего потому, что всем пациентам профилактически назначали НМГ. Положительная корреляция активности PPL с D-димерами указывает на их возможную роль в тромботической микроангиопатии, связанной с КОВИД. МЧ тромбоцитарного происхождения обеспечивают каталитическую поверхность для комплекса ферментов протромбиназы с последующим образованием тромбина и стимулированием экспрессии молекул эндотелиальной адгезии. Тем не менее, у тяжелых пациентов легочные микрососудистые тромбы не могли быть исключены отрицательными результатами КТЛА.
В заключении, предварительные результаты исследования впервые демонстрируют повышение активности PPL у пациентов с КОВИД-19 пневмонией, что возможно связанно с состояниями гипервоспаления и гиперкоагуляции. Наши результаты свидетельствуют о PPL как о потенциальном маркере воспалительного процесса прогрессирования КОВИД-19 пневмонии в ТРН, в то время как их роль как протромботического индекса нуждается в дополнительном выяснении.
Оригинальная статья: https://www.degruyter.com/view...