Некоторые якорные белки ингибируют ключевой метаболический драйвер, который играет важную роль в раковых заболеваниях и расстройствах развития мозга.
Ученые из Немецкого онкологического научного центра (DKFZ) и Инсбрукского университета вместе с общеевропейской исследовательской сетью открыли этот молекулярный механизм, который может предоставить новые возможности для индивидуализированной терапии онкологических и нейронных заболеваний. Результаты опубликованы в журнале Cell.
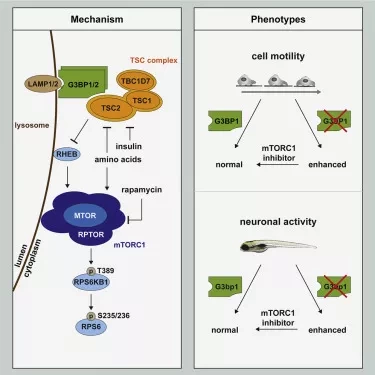
Сигнализирующий белок MTOR (Mechanistic Target of Rapamycin) является сенсором для таких питательных веществ, как аминокислоты и сахара. При наличии достаточного количества питательных веществ MTOR усиливает метаболизм и обеспечивает наличие достаточного количества энергии и клеточных строительных блоков. Так как MTOR является центральным переключателем метаболизма, ошибки в его активации приводят к серьезным заболеваниям. Раковые заболевания и нарушения развития нервной системы, приводящие к поведенческим расстройствам и эпилепсии, могут быть результатом неправильной работы MTOR.
Поэтому клетка очень точно контролирует активность MTOR с помощью так называемых супрессоров. Это молекулы, которые ингибируют белок и помогают регулировать его активность. Комплекс TSC является таким супрессором для MTOR. Он назван в честь болезни, которая вызывает его отсутствие - туберозный склероз (TSC). Комплекс TSC расположен вместе с MTOR в лизосомах клетки, где он держит под контролем MTOR. Если комплекс TSC - например, из-за изменения одного из его компонентов, больше не остается в лизосоме, это может привести к чрезмерной активности MTOR с тяжелыми последствиями для здоровья.
Поэтому специалисты исследовали, как комплекс TSC связывается с лизосомами. Они обнаружили, что белки G3BP (Ras GTPase-активирующий протеино-связывающий белок) находятся вместе с комплексом TSC в лизосомах. "Там белки G3BP образуют якорь, который обеспечивает связывание комплекса TSC с лизосомами", - объясняет Мирья Тамара Прентцелл из DKFZ, первый автор публикации. Эта якорная функция играет решающую роль в клетках рака молочной железы. Если количество белков G3BP в культурах клеток уменьшается, то это не только приводит к повышению активности MTOR, но и увеличивает миграцию клеток.
Препараты, которые ингибируют MTOR предотвращают это распространение, что исследователи смогли показать на клеточных культурах. У больных раком молочной железы низкий уровень G3BP коррелирует с худшим прогнозом. "Маркеры, такие как G3BP белки могут быть полезны для персонализации терапии на основе ингибирования MTOR", объясняет Катрин Тэддик, профессор биохимии в Университете Инсбрука. Хорошо то, что препараты, которые ингибируют MTOR, уже одобрены в качестве препаратов от рака и могут быть протестированы специально в дальнейших исследованиях.
Белки G3BP также ингибируют MTOR в мозге. На животных моделях исследователи наблюдали нарушения в развитии мозга при отсутствии G3BP. Это приводит к гиперактивности нейронов, похожей на эпилепсию у человека. Эти нейронные разряды могут быть подавлены препаратами, которые ингибируют MTOR.
"Поэтому мы надеемся, что пациенты с редкими наследственными неврологическими заболеваниями, в которых дисфункции белков G3BP играют определенную роль, могут выиграть от препаратов против MTOR", говорит Кристиан Опиц из DKFZ.