Ученые Йельского университета нашли способ "зарядить" атакующие опухоли Т-клетки, что может не только повысить эффективность перспективного вида клеточной иммунотерапии рака, но и расширить число видов рака, которые она может лечить.
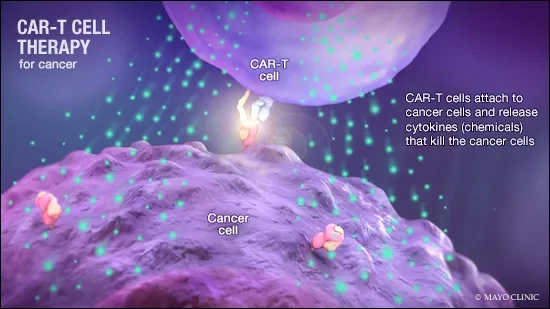
Результаты исследования опубликованы в журнале Cell Metabolism. Это открытие может способствовать развитию клеточной терапии CAR-T, которая использует иммунный ответ Т-клеток на раковые опухоли путем введения в клетки молекул, распознающих опухоль. За последнее десятилетие Управление по контролю за продуктами и лекарствами США одобрило шесть CAR-T клеточных терапий для лечения В-клеточных лимфом и множественной миеломы. Но, несмотря на первые успехи, эффективность лечения со временем снижается, что послужило началом поиска способов усиления функции Т-клеток. Кроме того, в настоящее время не существует одобренных методов лечения солидных опухолей с помощью CAR-T клеток.
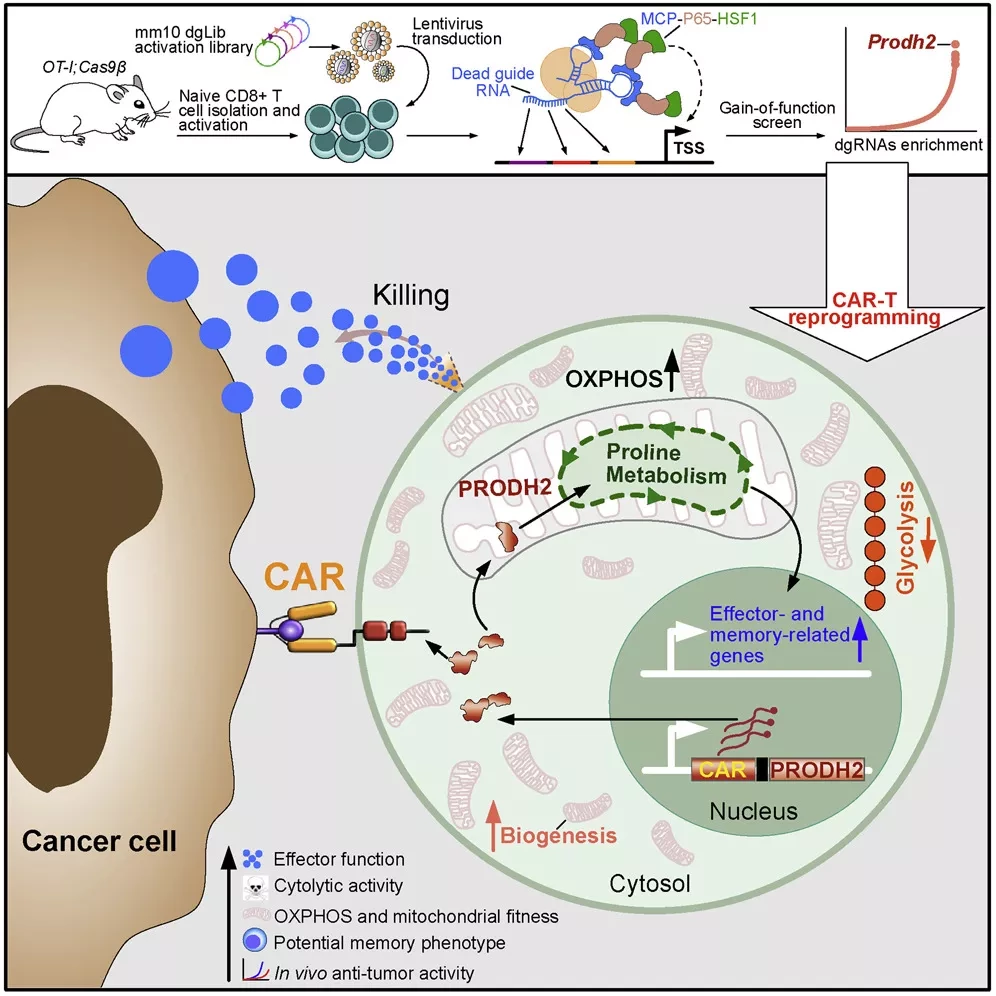
Для нового исследования ученые из лаборатории Сиди Чена, доцента генетики Йельского университета и старшего автора статьи, придумали оригинальный способ эффективного сканирования генома CD8 Т-клеток на наличие специфических генов, которые могут повысить способность клеток атаковать раковые клетки.
"Мы разработали новый вид геномного скрининга усиления функции, чтобы найти молекулярный фермент, который действует как педаль газа, повышая метаболическую активность в Т-клетках",
- рассказал Чен. Ученые обнаружили, что высокий уровень активности нескольких генов, включая PRODH2, гена, участвующего в клеточном метаболизме, стимулирует повышенную активность CAR-T клеток в мышиных моделях, используемых для изучения трех различных типов рака, включая рак молочной железы. Полученные результаты показывают возможность получения гиперметаболических CAR-T клеток, которые превосходят существующие методы клеточной терапии, говорят исследователи.
Используя эти системы и результаты, будущие исследования могут протестировать новые типы метаболически усиленных CAR-T клеток в клинических условиях, выявить другие "суперзаряженные" Т-клетки и распространить клеточную иммунотерапию на различные типы рака, особенно солидные опухоли, отметил Чен.
Lupeng Ye et al. Геномный скрининг усиления функций CRISPR в CD8 Т-клетках выявляет метаболизм пролина как средство для усиления CAR-T терапии (аннотация).
Иммунотерапия рака и иммунологических заболеваний на основе химерных антигенных рецепторов (CAR)-Т-клеток достигла больших успехов, но все еще сталкивается с многочисленными препятствиями. Поиск правильных молекулярных мишеней для инженерии Т-клеток с целью выполнения желаемой функции имеет широкие последствия для арсенала Т-клеточной терапии. В данном исследовании мы разработали скрининг активации на основе технологии CRISPR dead-guide RNA (dgRNA) в первичных CD8+ Т-клетках и определили мишени усиления функции (GOF) для CAR-T инженерии. Целенаправленное нокаутирование или сверхэкспрессия ведущей мишени, PRODH2, усилила киллинг на основе CAR-T и эффективность in vivo в нескольких моделях рака. Транскриптомика и метаболомика в CAR-T клетках показала, что усиление экспрессии PRODH2 изменило широкие и различные программы экспрессии генов и метаболизма. Митохондриальный, метаболический и иммунологический анализы показали, что инженерия PRODH2 усиливает метаболические и иммунные функции CAR-T клеток против рака.
Вместе эти результаты обеспечивают систему идентификации иммуноусилителей GOF и демонстрируют PRODH2 в качестве мишени для повышения эффективности CAR-T.