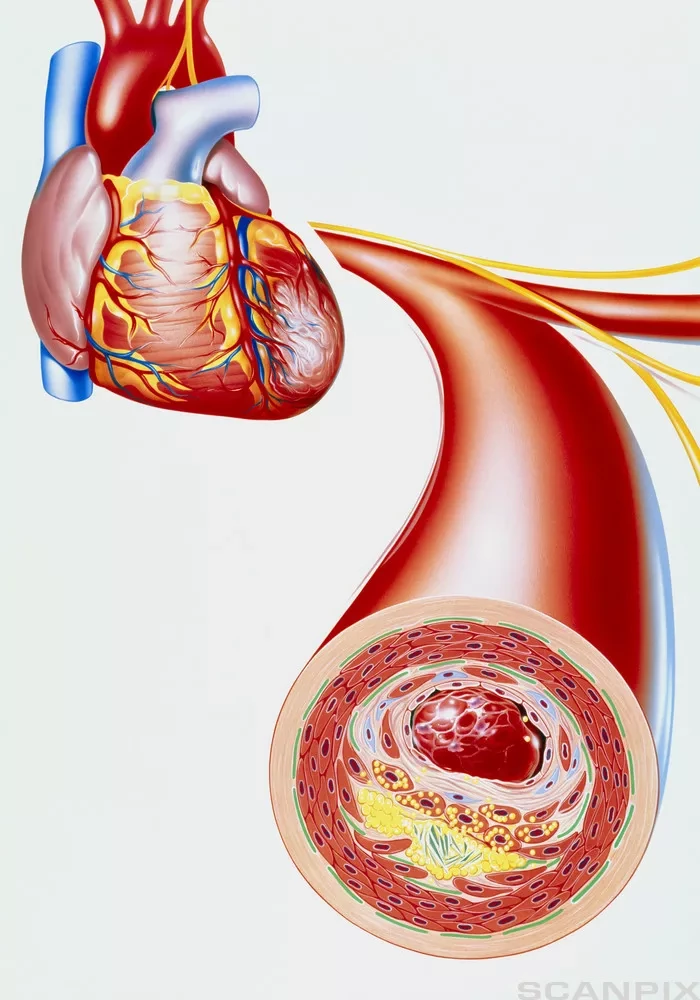
Исследователи изучили образцы аутопсии тканей сердца пациентов, умерших в начале пандемии COVID-19.
Как и ожидалось, в сосудах сердца были обнаружены частые и обширные тромбозы, однако изменения в эндотелиальных клетках, выстилающих сердце, которые обычно наблюдаются при тромбозах, отсутствовали. Вместо этого данные указывали на то, что вероятным виновником является гиперкоагуляция крови, вызванная активированными нейтрофилами. Результаты исследования опубликованы в журнале The American Journal of Pathology.
"Моя лаборатория давно занимается определением изменений эндотелиальных клеток, которые приводят к патологиям, включая тромбоз, и мы ожидали подтвердить широко распространенное предположение о том, что местные изменения эндотелиальных клеток ответственны за тромбоз сердечных сосудов у пациентов COVID-19", - пояснил ведущий исследователь Джордан С. Побер.
"Вместо этого мы обнаружили, что сердечные тромбы содержали нейтрофилы, которые экспрессировали изменения стимулирующие коагуляцию, включая изменения, связанные с гибелью клеток и воспалением".
Госпитализированные пациенты с инфекцией SARS-CoV-2 имеют повышенный риск развития поражения миокарда. Однако многочисленные исследования редко выявляли вирусный белок или РНК в сердцах пациентов, умерших от COVID-19, несмотря на доказательства обильного присутствия вируса в легких тех же пациентов. Тромбоз микро- и макрокоронарных сосудов наиболее характерен для сердец людей, умерших от COVID-19, но основная причина остается неизвестной.
Побер и его коллеги изучили ткани сердца из семи аутопсий пациентов с COVID-19, проведенных в начале пандемии, до того, как обычно применялось антикоагуляционное лечение, и сравнили эти образцы с тканями аутопсий 12 пациентов с COVID-19 - отрицательным контролем, с заболеваниями сердца и без них, используя многопараметрическую флуоресцентную микроскопию для анализа состава тромбированных сосудов. У всех пациентов в группе COVID-19 была тяжелая пневмония. У одного пациента произошла внезапная остановка сердца за пределами больницы, у двух пациентов развился сепсис, а у одного - рецидивирующий острый лейкоз с тромбоцитопенией. В группу COVID-19-отрицательного контроля вошли шесть пациентов с уже существующими сердечными заболеваниями.
Тромбоз был наиболее распространенной патологической находкой в группе COVID-19 со значительно повышенной частотой микротромбов и общим количеством макротромбов по сравнению с COVID-19-отрицательным контролем. Несмотря на широко распространенные признаки тромбоза, в группе COVID-19 не было обнаружено признаков гибели миоцитов или острого воспаления, обычно ассоциируемого с инфарктом миокарда.
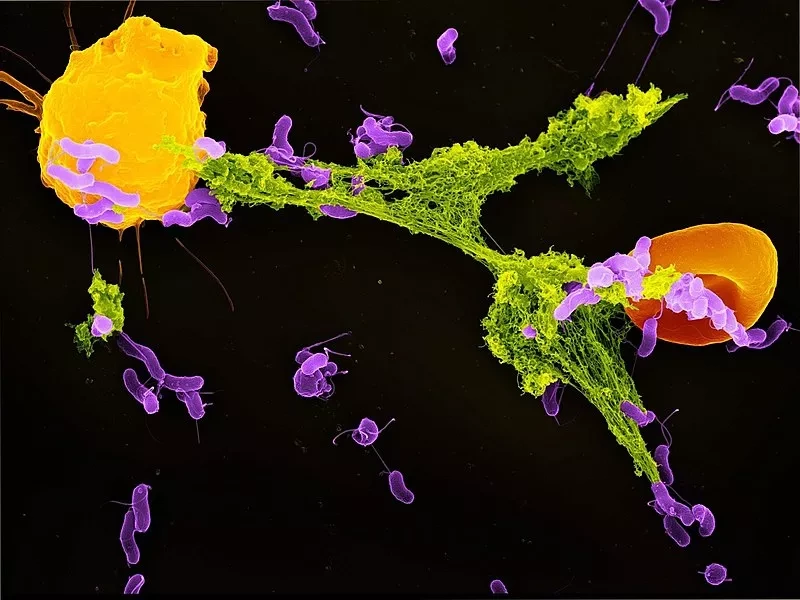
Сосуды сердца были исследованы на наличие признаков повреждения эндотелиальных клеток, которое может способствовать тромбозу за счет высвобождения микрочастиц, содержащих прокоагуляционный тканевой фактор, или за счет слущивания эндотелиальных клеток, которое может обнажить коллаген, активирующий тромбоциты. Исследователям не удалось обнаружить таких эндотелиальных изменений в местах тромбоза. Вместо этого они увидели, что сердечные тромбы у четырех из шести пациентов COVID-19 содержали нейтрофилы, которые выражали прокоагулянтные изменения в крови, такие как цитруллинизация гистонов, связанная с образованием внеклеточных ловушек нейтрофилов (NETs). На некоторых изображениях видны NETS, которые, по-видимому, непосредственно связаны с тромбоцитами. Богатые нейтрофилами макротромбы, состоящие из 30% и более нейтрофилов, были распространены в группе COVID-19, но не в контрольных образцах тканей.
Побер прокомментировал: "Наши данные опровергают мнение о том, что изменения в стенке сосудов сердца являются основной причиной сердечного тромбоза при COVID-19. Современные методы лечения тяжелой формы COVID-19 включают антикоагулянты, но оптимальная стратегия до сих пор не ясна. В свете полученных нами результатов снижение реакции нейтрофилов может стать важной мишенью для терапевтического вмешательства. Этот и многие другие достижения в понимании болезни по-прежнему обеспечиваются аутопсиями, и я благодарен патологоанатомам, проводившим их для этого исследования".
"В течение нескольких лет мы изучали нейтрофилы и их протромботические продукты, известные как NETs, в контексте тромбов, образующихся в крупных коронарных артериях. Обнаружение участия нейтрофилов в более мелких кровеносных сосудах, проходящих через сердечную мышцу в COVID-19, расширяет наше понимание повреждения сердца, которое мы часто наблюдаем у пациентов с тяжелой инфекцией SARS-CoV-2".
Justin E. Johnson et al. Тромбоз коронарных сосудов при COVID-19 (аннотация).
Тяжелая коронавирусная болезнь 2019 (COVID-19) повышает риск повреждения миокарда, что способствует увеличению летальных исходов. В данном исследовании использовалась многопараметрическая иммунофлуоресценция для всестороннего изучения аутопсийных тканей сердца 7 пациентов, умерших от COVID-19, по сравнению с 12 контрольными образцами, с сердечно-сосудистыми заболеваниями или без них. В соответствии с предыдущими сообщениями, не было обнаружено никаких признаков вирусной инфекции или лимфоцитарной инфильтрации, свидетельствующей о миокардите. Однако в сердцах пациентов из когорты COVID-19 наблюдались частые и обширные тромбозы в крупных и мелких сосудах, что было редкостью для контрольных образцов.
Эндотелиальная выстилка тромбированных сосудов обычно не имела признаков цитокинопосредованной активации эндотелия, оцениваемой по ядерной экспрессии транскрипционных факторов p65 (RelA), pSTAT1 или pSTAT3, или признаков воспалительной активации, оцениваемой по экспрессии молекулы внутриклеточной адгезии-1 (ICAM-1), молекулы адгезии сосудистых клеток-1 (VCAM-1), тканевого фактора или фактора фон Виллебранда (VWF). Интимальная выстилка EC также была в целом сохранена с небольшими признаками гибели клеток или десквамации. Напротив, у пациентов с COVID-19 в тромбах миокарда часто встречались маркеры активации нейтрофилов, включая агрегаты нейтрофилов с тромбоцитами, богатые нейтрофилами скопления в макротромбах и признаки образования внеклеточных ловушек нейтрофилов (NET).
Эти данные указывают на изменения в циркулирующих нейтрофилах, а не в эндотелии, как на фактор, способствующий увеличению тромботического диатеза в сердцах пациентов с COVID-19.