Рак легких имеет самый высокий уровень смертности среди всех видов рака, а возможности его лечения крайне ограничены, особенно для пациентов с онкогенными мутациями в гене KRAS.
Большие надежды возлагались на лицензирование ингибиторов иммунных контрольных точек, но реальность такова, что некоторые пациенты очень хорошо реагируют на это лечение, в то время как у других оно совершенно неэффективно. В работе, опубликованной в журнале Science Translational Medicine, исследовательская группа MedUni Vienna под руководством Хервига Молля (Центр физиологии и фармакологии) определила потенциальный маркер успеха иммунотерапии у пациентов с раком легких и объяснила лежащие в ее основе молекулярные процессы.
K-Ras - это мономерный G-белок, который играет ключевую роль в росте злокачественных опухолей. Мутировавшие KRAS карциномы легких часто возникают в хронически воспаленных легких, особенно у заядлых курильщиков. Воспалительные процессы способствуют росту раковых клеток. Исследовательская группа показала, что экспрессия сильного противовоспалительного белка A20, образующегося в самом организме, часто очень низка в этих злокачественных клетках, и что существует прямая зависимость между продолжительностью жизни пациента и экспрессией этого белка. Молл объясняет:
"Как у людей, так и в животной модели, потеря A20 приводит к снижению иммунного контроля за раковыми клетками. Раковые клетки с низким уровнем А20 способны избегать обнаружения иммунной системой. Это приводит к значительному ускорению роста опухоли".
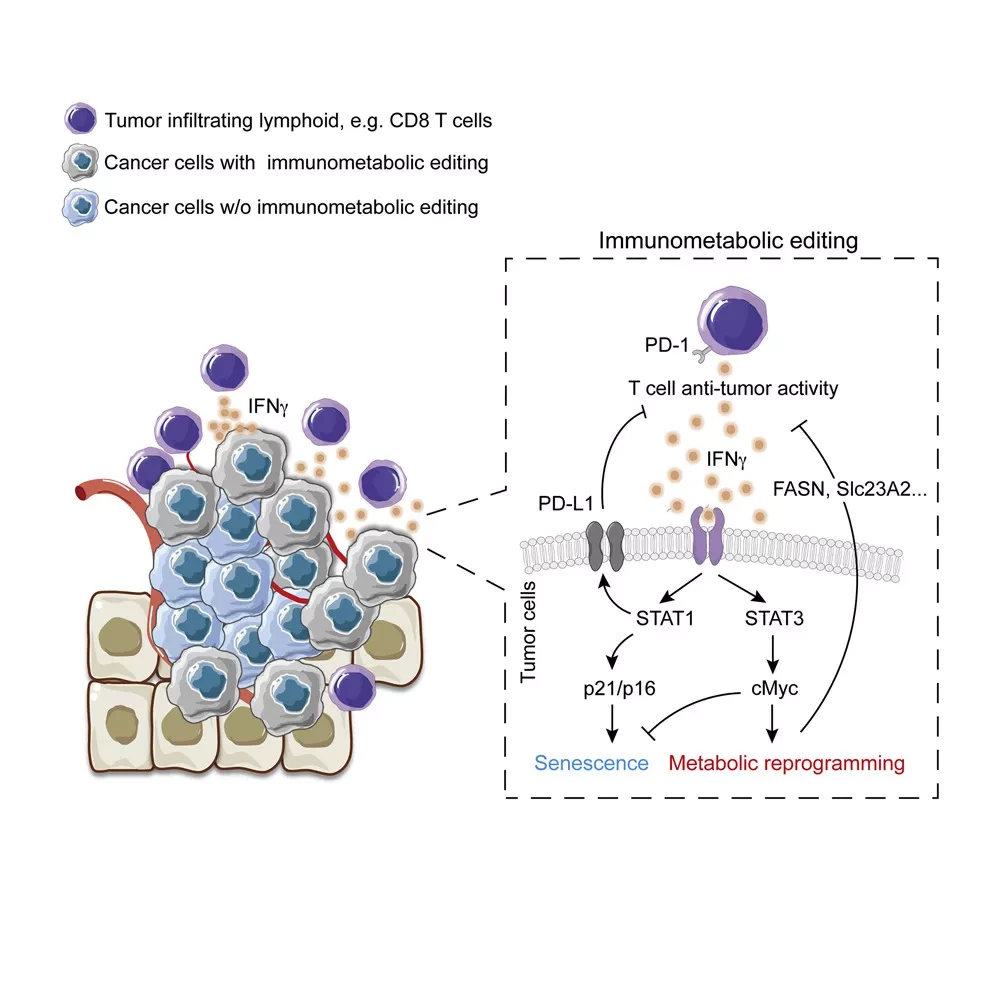
В ходе исследования было обнаружено, что за это отвечает прежде всего повышенная чувствительность раковых клеток к иммуномодулирующему цитокину гамма-интерферону. Более того, опухолевые клетки с пониженным уровнем A20 особенно хорошо реагировали на ингибиторы иммунных контрольных точек, точно так же, как и в случае пациентов, страдающих меланомой (раком кожи) с аналогичной структурой экспрессии генов.
"В A20 мы обнаружили ранее неизвестный опухолевый супрессор при раке легких, потеря которого в качестве иммунного чекпойнта способствует развитию этого злокачественного заболевания", - объясняет соавтор исследования Эмилио Казанова. Поскольку у пациентов с низкой экспрессией A20 мало иммунных клеток, борющихся с опухолью, и поэтому на поздних стадиях они экспрессируют мало важной иммунной контрольной молекулы PD-L1, эти пациенты могут быть исключены из иммунотерапии, направленной против PD-L1. Действительно, интенсивность экспрессии этой молекулы в настоящее время рассматривается в качестве вспомогательного фактора при принятии решения о необходимости лечения ингибиторами иммунных контрольных точек. "Основываясь на наших результатах и данных, полученных от пациентов с меланомой, мы убеждены, что выявили группу пациентов с раком легких, которым действительно будет полезна эта иммунотерапия. Исключение из такого лечения значительно снизит выживаемость таких пациентов".
В ходе дальнейшего исследования ученые хотят выяснить, можно ли манипулировать экспрессией A20 в раковых клетках, чтобы усилить эффект иммунотерапии. "Тем не менее, курение по-прежнему является наиболее легко устранимым фактором риска развития рака легких. Поэтому мы должны поддерживать законы, защищающие население от вдыхания вредного дыма, и в то же время призывать людей к личной ответственности за полное воздержание от курения", - говорит Молл. Тем не менее, важно продолжать исследовать новые терапевтические подходы для улучшения качества жизни и повышения шансов на выживание больных.
Kristina Breitenecker et al. Снижение регуляции A20 способствует иммунному уходу аденокарциномы легких (аннотация).
Воспаление является хорошо известной движущей силой опухолеобразования в легких. Одна из стратегий, с помощью которой опухолевые клетки избегают жесткого гомеостатического контроля, заключается в снижении экспрессии мощного противовоспалительного белка фактора некроза опухоли альфа-индуцированного белка 3 (TNFAIP3), также известного как A20. Мы наблюдали, что потеря A20, присущая опухолевым клеткам, заметно усиливала опухолегенез легких и была связана со снижением иммунного надзора, опосредованного CD8+ T-клетками, у пациентов с раком легких и в мышиных моделях. У мышей мы наблюдали, что этот эффект полностью зависит от повышенной чувствительности клеток к сигналу интерферона-γ (IFN-γ) путем аберрантной активации TANK-связывающей киназы 1 (TBK1) и повышенной экспрессии и активации сигнального трансдуктора и активатора транскрипции 1 (STAT1).
Прерывание этой аутокринной прямой петли путем отключения рецептора IFN-α/β полностью восстановило инфильтрацию цитотоксических Т-клеток и устранило потерю A20-зависимого опухолевого генеза. В опухолях легких, нокаутных по А20, высоко экспрессировался лиганд программируемой смерти 1 (PD-L1). Соответственно, лечение блокадой иммунных контрольных точек (ICB) было высокоэффективным у мышей, у которых были опухоли легких с дефицитом A20. Более того, сигнатура экспрессии генов с потерей функции A20 положительно коррелировала с выживаемостью пациентов с меланомой, получавших антипрограммированный белок клеточной смерти 1.
В совокупности мы определяем A20 в качестве главного иммунного контрольного пункта, регулирующего ось TBK1-STAT1-PD-L1, который может быть использован для улучшения терапии ICB у пациентов с аденокарциномой легких.