Клиническое исследование обнаружило биомаркер действия глюкокортикоидов, который может быть использован для разработки тестов и помощи клиницистам в адаптации лечения.
Согласно исследованию, опубликованному в eLife, обнаружены механизмы, участвующие в реакции организма на лечение глюкокортикоидами (ГК), и определен новый биомаркер, который можно использовать для контроля за тем, как эти лекарства работают у пациентов. Более надежный показатель ответа индивидуума на ГК препараты мог бы быть использован для разработки клинически применимого теста для адаптации терапии и потенциальной минимизации побочных эффектов.
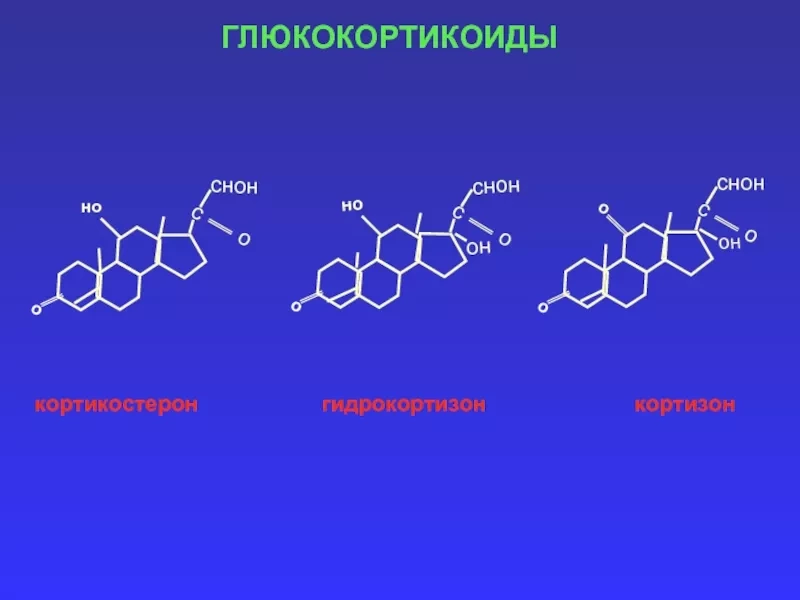
ГК, такие как кортизол, являются одним из гормонов, играющих ключевую роль в реакции организма на стресс. ГК препараты являются одним из наиболее часто назначаемых методов лечения при различных заболеваниях, в том числе для пациентов, у которых надпочечники не в состоянии вырабатывать достаточное количество кортизола. Действие ГК является сложным, что означает, что уровень кортизола в крови не отражает достоверно то, что происходит в тканях. Это усложняет задачу для медицинских работников в вопросе адаптации методов терапии.
Тем не менее, до сих пор нет биомаркера, который мог бы количественно оценить действие ГК. Целью исследования являлось выявление и валидация циркулирующих биомаркеров глюкокортикоидного действия путем определения мультиомных паттернов, полученных из отдельных тканей, связанных с действием ГК, и использование этих паттернов для поиска клинически применимых циркулирующих биомаркеров действия ГК.
"Побочные эффекты лечения ГК часто наблюдаются у пациентов, что указывает на неадекватность существующих методов контроля их действия, которые обычно направлены на клиническую реакцию или активность заболевания", - объясняет первый автор Димитриос Шанцихристос. "Мы хотели найти некий биомаркер, который можно было бы замерять и контролировать действие ГК, надеясь, что это поможет врачам понять, как лучше всего лечить пациентов".
В рандомизированном, перекрестном, одиночном слепом, исследовании наблюдались 10 пациентов с первичной адреналиновой недостаточностью (болезнью Эддисона) (и без других эндокринопатий) во время физиологического воздействия и прекращения терапии ГК. Вместо того, чтобы сосредоточиться только на метаболических продуктах, связанных с воздействием ГК, исследователи также изучили экспрессию генов и микроРНК у пациентов, используя новые компьютерные модели. Эти различные факторы были проанализированы в клетках крови и жировой ткани, важной метаболической среде, где меняется уровень кортизола, выявив тесную взаимосвязь между различными элементами, вовлеченными в действие ГК. Транскриптом в мононуклеарных клетках периферической крови и жировой ткани, плазменные микроРНК и сывороточные метаболиты сравнивали между собой с помощью интегрированного мультиомного анализа. Это позволило исследователям сравнить активность в тканях одних и тех же пациентов при низких уровнях кортизола и после ГК терапии, помогая объяснить различия между индивидуумами.
В результате определения транскриптомного профиля, среди идентифицированных ими элементов была выявлена микроРНК (miR-122-5p), коррелирующая с генами и метаболитами, которые регулируются ГК. Для подтверждения этой корреляции специалисты изучили результаты трех независимых исследований, в процессе которых определялся уровень miR-122-5p в крови пациентов, проходящих терапию ГК, и нашли эту же закономерность, подтверждая гипотезу о том, что эта микроРНК может быть полезным биомаркером действия ГК.
Полученные результаты создают основу для успешного открытия биомаркеров для измерения эффекта действия ГК, позволяя индивидуализировать и оптимизировать ГК терапию, и проливают свет на этиологию заболеваний, связанную с нефизиологическим воздействием ГК, как, например, при сердечно-сосудистых заболеваниях и ожирении.
"Этот потенциальный биомаркер теперь может быть исследован в больших группах пациентов с целью разработки клинически применимого теста", - заключает Шанцихристос.