Эволюция обеспечила нам определенный уровень защиты от экзистенциальной угрозы холодной температуры благодаря способности вырабатывать тепло из жира, хранящегося в организме.
Однако с возрастом люди становятся более восприимчивыми к холоду, а также к воспалениям и метаболическим проблемам, которые могут привести к множеству хронических заболеваний. Исследователи из Йельского университета и Университета Калифорнии - Сан-Франциско (UCSF) обнаружили одного виновника этого процесса - те самые иммунные клетки в жировой ткани, которые призваны защищать нас от низких температур.
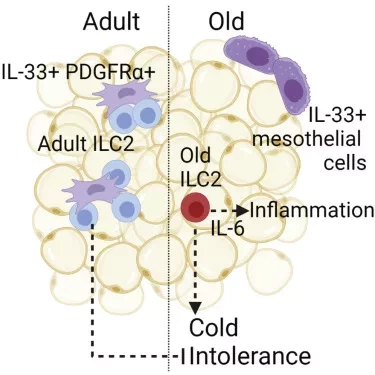
В новом исследовании они обнаружили, что жировая ткань старых мышей теряет иммунные клетки группы 2 врожденных лимфоидных клеток (ILC2), которые восстанавливают тепло тела при воздействии низких температур. Но в качестве предостережения для тех, кто ищет легкие методы лечения болезней старения, они также обнаружили, что стимулирование производства новых клеток ILC2 у стареющих мышей фактически делает их более склонными к смерти от холода. "То, что полезно для вас в молодости, может стать губительным для вас с возрастом", - сказал Вишва Дип Диксит, профессор сравнительной медицины и иммунобиологии имени Вальдемара фон Зедтвица и соавтор исследования. Результаты исследования опубликованы в журнале Cell Metabolism.
Диксит и коллеги изучали, почему жировая ткань содержит клетки иммунной системы, которые обычно сосредоточены в местах, часто подверженных воздействию патогенов, таких как носовые ходы, легкие и кожа. Когда они секвенировали гены из клеток старых и молодых мышей, то обнаружили, что у старых животных не хватает клеток ILC2, что ограничивает их способность сжигать жир и повышать температуру тела в холодных условиях. Когда ученые ввели молекулу, повышающую выработку ILC2 у стареющих мышей, клетки иммунной системы восстановились, но мыши, на удивление, стали еще менее устойчивы к низким температурам.
"Простое предположение заключается в том, что если мы восстановим что-то утраченное, то мы также вернем жизнь в нормальное русло", - сказал Диксит. " Но этого не произошло. Вместо того, чтобы увеличивать количество здоровых клеток молодости, фактор роста в итоге привел к размножению плохих клеток ILC2, которые остались в жире старых мышей". Но когда исследователи взяли клетки ILC2 у молодых мышей и пересадили их пожилым мышам, они обнаружили, что способность пожилых животных переносить холод восстанавливается.
"Иммунные клетки играют роль не только в защите от патогенов, но и помогают поддерживать нормальные метаболические функции",
- отметил Диксит. "С возрастом иммунная система уже изменилась, и мы должны быть осторожны в своих манипуляциях с ней для восстановления здоровья пожилых людей".
Emily L.Goldberg et al. IL-33 вызывает термогенную недостаточность при старении путем наращивания дисфункциональных жировых ILC2 (аннотация).
Старение нарушает интегрированные иммунометаболические реакции, которые эволюционировали для поддержания основной температуры тела у гомеотермов, чтобы выжить при холодовом стрессе, инфекциях и ограничении питания. Воспаление жировой ткани регулирует термогенный стрессовый ответ, но как клетки, обитающие в жировой ткани, провоцируют термогенный сбой у пожилых людей, неизвестно.
В данном исследовании мы определили изменения в иммунной системе жировой ткани и установили, что врожденные лимфоидные клетки второго типа (ILC2s) теряются при старении. Восстановление количества ILC2 у пожилых мышей до уровня, наблюдаемого у взрослых особей, путем введения IL-33 не спасло старых мышей от метаболических нарушений и повышенной летальности, вызванной холодом. Транскриптомный анализ выявил внутренние дефекты в пожилых ILC2, а адоптивный перенос взрослых ILC2 достаточен для защиты старых мышей от холода.
Таким образом, функциональные дефекты в жировых ILC2 при старении приводят к термогенной недостаточности.