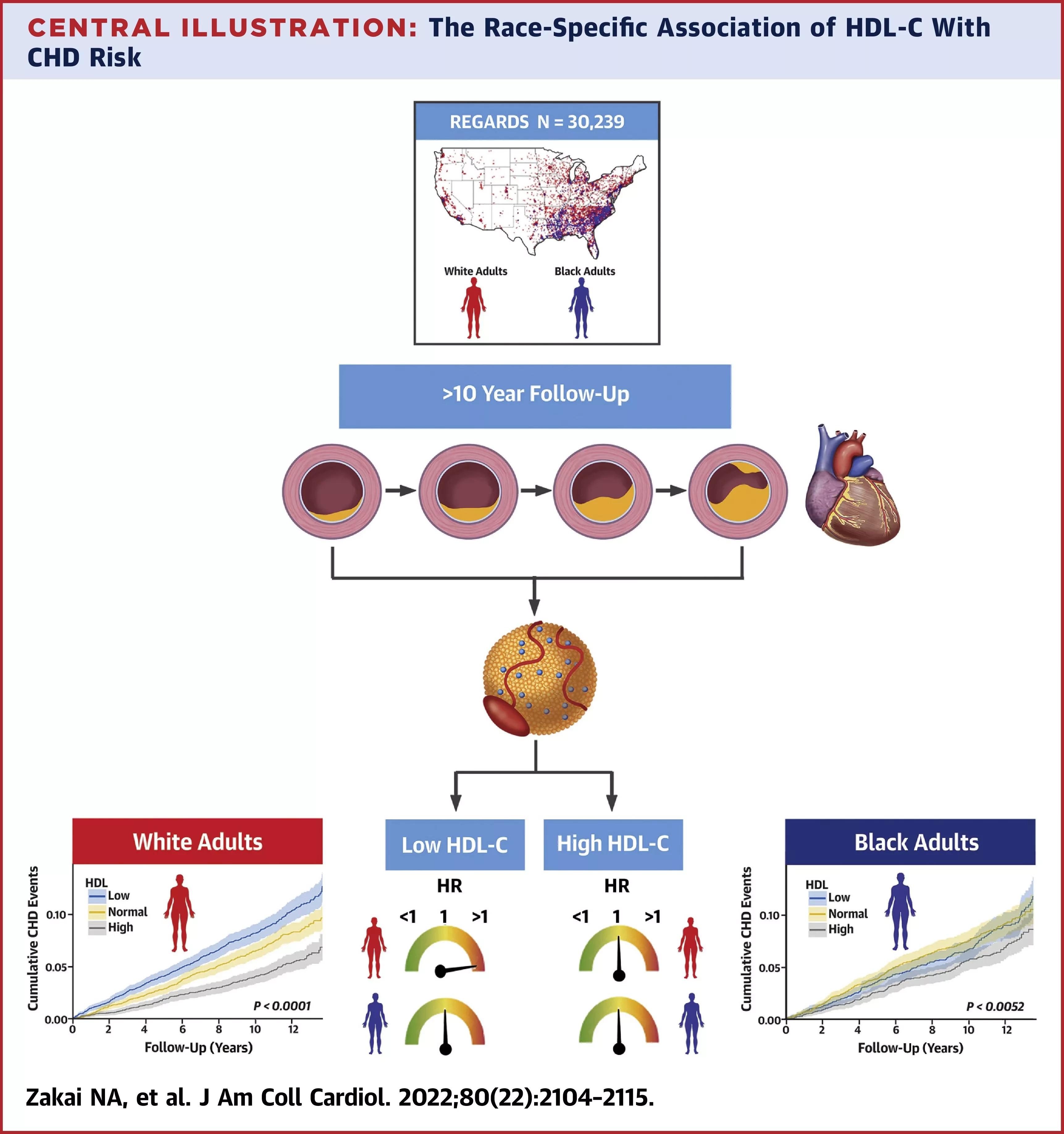
Тип подготовки иммунных клеток, называемый тренированным иммунитетом, помогает исследователям понять механизмы болезни, лежащие в основе накопления атеросклеротических отложений.
Большинство сердечно-сосудистых событий начинается с атеросклероза - состояния, при котором воспаление и жировые отложения вызывают сужение и ригидность артерий. Эти отложения, или бляшки, накапливаются годами. Когда они смещаются и попадают в более мелкие сосуды, они могут перекрыть кровоток к жизненно важным органам, вызывая инфаркты и инсульты.
Хотя многие факторы, способствующие развитию атеросклероза, включая высокий уровень холестерина и гипертонию, хорошо изучены, их устранение не снижает риск развития заболевания. "Липидоснижающие препараты снижают риск сердечно-сосудистых заболеваний только примерно на 35%, поэтому существует огромный пробел, который мы оставляем без лечения", - говорит Эстер Лютгенс, изучающая сосудистую иммунологию в Амстердамском университете. По ее словам, за последние несколько десятилетий исследователи поняли, что устранение воспаления может стать способом восполнить этот пробел. В конце концов, сердечно-сосудистые заболевания чаще встречаются у людей с хроническими воспалительными заболеваниями, такими как ревматоидный артрит и хроническая инфекция десен.
Теперь тип иммунной памяти, так называемый тренированный иммунитет, предлагает исследователям биологический механизм, объясняющий некоторые из этих связей, а также предлагает новые мишени для лекарственных препаратов. Тренированный иммунитет возникает во врожденных иммунных клетках. Эти клетки не формируют память в классическом смысле этого слова, создавая рецепторные белки, которые связываются с конкретными патогенами. Вместо этого они запоминают предыдущие воздействия через изменения в своих генах и метаболизме. "Когда эти клетки в будущем сталкиваются со стимулом, связанным или не связанным с первоначальным, они могут реагировать быстрее и сильнее", - говорит Джордж Хаджишенгаллис, иммунолог из Университета Пенсильвании в Филадельфии.
Исследователи показали, что патогены, гормоны стресса и холестерин могут тренировать иммунные клетки, которые, как известно, играют важную роль в развитии атеросклероза. Теперь они проверяют, может ли тренированный иммунитет быть механистическим звеном между воспалительными заболеваниями и атеросклерозом. "Это действительно дает возможность найти механизм, который может объяснить некоторые из предыдущих выводов о том, как факторы риска приводят к долгосрочному эффекту при атеросклерозе. И очень интересную основу, которая может быть использована в будущем для разработки новых лекарств", - говорит Нильс Риксен, специалист по сосудистой медицине из Университета Радбоуда в Неймегене, Нидерланды.
Риксен тесно сотрудничает с группой исследователей из Радбоуда, которые десять лет назад впервые описали тренированный иммунитет. Они обнаружили, что воздействие определенных грибков или бактерий вызывает у клеток врожденного иммунитета, включая моноциты и макрофаги, появление эпигенетических меток на гистонах - изменений в белках, которые связывают и хранят ДНК, но не влекут за собой изменения основного кода ДНК. Эти изменения позволили клеткам быстро получить доступ к ключевым генам, участвующим в воспалении и метаболизме, и впоследствии быстро активизировать иммунный ответ на любой раздражитель.
После десятилетия работы было показано, как тренированный иммунитет защищает клетки, животных и людей от инфекций. Но с самого начала Риксен подозревал, что это явление не может быть однозначно полезным. В конце концов, моноциты и макрофаги усугубляют атеросклероз. Когда моноциты сталкиваются с атеросклеротической бляшкой на стенке кровеносного сосуда, они превращаются в макрофаги и выделяют вызывающие воспаление молекулы, называемые цитокинами. Макрофаги также выделяют ферменты, которые разъедают белок и заставляют бляшки распадаться на кусочки, которые могут блокировать кровоток. В этом контексте, считает Риксен, гиперреактивные тренированные моноциты или макрофаги могут быть вредны.
В 2012 году Риксен привлек тогдашнего аспиранта Сирона Беккеринга, иммунолога из Радбоуда, к поиску связей между тренированным иммунитетом и атеросклерозом. Беккеринг начала с дозирования человеческим моноцитам двух типов холестерина: липопротеина низкой плотности (ЛПНП), который часто называют "плохим" холестерином, и его окисленной формы, oxLDL. Она обнаружила, что oxLDL вызывает эпигенетические изменения, которые позволяют клеткам производить больше цитокинов после того, как они подверглись воздействию не связанного с ними соединения, стимулирующего иммунитет. То есть холестерин может вызывать тренированный иммунитет - по крайней мере, в клетках.
Чтобы проверить это на людях, группа исследовала моноциты 20 человек с тяжелой формой атеросклероза. Клетки имели все признаки тренированного иммунитета, включая повышенный цитокиновый ответ, эпигенетические изменения и изменения в генах, связанных с метаболизмом. В исследовании, опубликованном другой группой в том же году, были получены аналогичные результаты.
Все фрагменты вставали на свои места. Риксен говорит, что некоторые из самых прямых доказательств были получены при изучении людей с семейной гиперхолестеринемией - генетическим заболеванием, вызывающим высокий уровень холестерина в крови. Беккеринг обнаружил, что моноциты 25 человек с этим заболеванием имели характерные признаки тренированности, которые сохранялись в течение трех месяцев после того, как они начали принимать препараты, снижающие уровень холестерина, называемые статинами. Это состояние повышает риск сердечно-сосудистых заболеваний, и этот риск не исчезает полностью при приеме статинов. Риксен говорит, что, возможно, тренированный иммунитет поддерживает воспаление еще долгое время после начала лечения. Группа следит за участниками исследования в надежде выяснить, можно ли обратить вспять или предотвратить развитие тренированного иммунитета.
Моноциты циркулируют в организме всего несколько дней, после чего выводятся из организма и заменяются. Поэтому для того, чтобы тренированный иммунитет сохранялся в течение нескольких месяцев, он должен воздействовать и на стволовые клетки-предшественники моноцитов в костном мозге. За последние несколько лет исследования на мышах и людях показали, что вакцина против туберкулеза вызывает тренированный иммунитет в стволовых клетках костного мозга, который сохраняется не менее года.
В прошлом году группа Риксена нашла доказательства того, что то же самое может быть справедливо и для ишемической болезни сердца. Исследователи проанализировали образцы костного мозга 13 человек с тяжелой формой атеросклероза и обнаружили, что некоторые воспалительные гены были более активны в стволовых клетках-предшественниках моноцитов этих 13 человек, чем у здоровых людей. Они также обнаружили изменения в метаболизме стволовых клеток, которые соответствовали тренированному иммунитету. Сейчас специалисты изучают модификации гистонов в клетках.
Концепция, согласно которой тренированный иммунитет может влиять на стволовые клетки, убедительно объясняет связь между атеросклерозом и воспалительными заболеваниями, такими как хронические заболевания десен и ревматоидный артрит.
По словам Хаджишенгаллиса, цитокины, вырабатываемые в результате этих заболеваний, легко достигают костного мозга, теоретически создавая долгоживущие запасы обученных моноцитов, которые могут способствовать воспалению в любой части тела.
"Это концепция с большой объяснительной силой", - говорит Хаджишенгаллис. Хотя ученые уже сделали много ключевых наблюдений, указывающих на тренированный иммунитет, "мы не знали, как соединить все точки", - говорит он. Сейчас группа Хаджишенгаллиса проверяет, может ли пародонтит, тяжелая инфекция десен и челюстной кости, вызывать тренированный иммунитет и способствовать развитию атеросклероза у мышей.
Тренированный иммунитет может также объяснить, почему перенесенное воспаление повышает риск сердечных заболеваний. Дэвид Бургнер, специалист по педиатрическим инфекционным заболеваниям из Детского научно-исследовательского института Мердока в Мельбурне, Австралия, в ходе крупных проспективных исследований обнаружил, что тяжелые инфекции в раннем возрасте повышают риск развития атеросклероза в дальнейшем. По его словам, встреча с Беккерингом на конференции в 2016 году была похожа на поиск недостающих кусочков головоломки.
Бургнер и Беккеринг объединили усилия для поиска признаков тренированного иммунитета после воспаления в матке и в раннем возрасте. До 70% преждевременных родов сопровождаются инфекцией оболочек, окружающих плод, называемой хориоамнионитом. Исследователи имитировали эту инфекцию у мышей с генетической предрасположенностью к атеросклерозу и обнаружили, что у мышей, перенесших воспаление как до, так и после рождения, атеросклеротические бляшки во взрослом возрасте были гораздо больше. Сейчас они ищут маркеры тренированного иммунитета в клетках врожденного иммунитета из пуповинной крови матерей с хориоамнионитом, родивших преждевременно.
Бургнер также проводит несколько исследований, чтобы выяснить, как инфекция вписывается в общую картину риска развития атеросклероза и сердечно-сосудистых заболеваний. "Я подозреваю, что на многие из этих традиционных факторов риска влияет воспаление, и интенсивность воспаления, которое они вызывают, является наследием того, что было раньше", - говорит он. "Я подозреваю, что большую часть этого в раннем возрасте составляет инфекция".
По мере того как исследователи определяют биологию, лежащую в основе тренированного иммунитета, они также выявляют потенциальные мишени для лекарств. В исследованиях вакцинации и инфекций тренированный иммунитет можно предотвратить, блокируя определенные модификации гистонов или ферменты, участвующие в метаболизме глюкозы. Сотрудники группы Риксена тестируют некоторые из этих подходов на мышиных моделях атеросклероза. Однако, поскольку все клетки используют гликолиз и модифицируют гистоны, исследователи также ищут способы воздействия на эти процессы конкретно в моноцитах и их предшественниках.
Виллем Малдер, биомедицинский инженер, который в январе перевел свою лабораторию в Радбоуд, работает с наноразмерными частицами, состоящими в основном из липопротеинов, которые легко поглощаются моноцитами и макрофагами и могут быть использованы для переноса лекарств. В 2019 году Малдер стал соучредителем биотехнологической фирмы Trained Therapeutix Discovery в Люксембурге для разработки таких нанобиологических препаратов для использования против тренированного иммунитета.
Некоторые из соединений, которые перспективны для блокирования тренированного иммунитета, включают ингибиторы, снижающие уровень интерлейкина-1β, цитокина, который, как известно, играет роль в сердечно-сосудистых заболеваниях, а также препараты, уже используемые для лечения сердечно-сосудистых заболеваний и других состояний - например, статины и метформин.
До сих пор компания фокусировалась на использовании частиц для доставки лекарств, которые либо усиливают, либо блокируют тренированный иммунитет при раке или после трансплантации органов, но он говорит, что эту же технологию можно адаптировать для лечения сердечно-сосудистых заболеваний. Он прогнозирует, что наибольшее влияние технология окажет при использовании после сердечного приступа, инсульта или тяжелой инфекции для предотвращения тренированного иммунитета и тем самым снижения риска будущих сердечных событий. В сотрудничестве с Национальным институтом аллергии и инфекционных заболеваний США группа Малдера сейчас проверяет, могут ли препараты, предотвращающие тренированный иммунитет, снизить риск сердечных событий после инфицирования вирусом SARS-CoV2 у макак-резусов с высоким уровнем холестерина.
По словам Беккеринг, лекарства, которые предотвращают иммунную тренировку, не обязательно отменяют ее. Действительно, ее исследование с участием людей с гиперхолестеринемией показывает, что статины не могут отменить тренировку в клетках человека. Есть намеки на то, что другие вмешательства могут отменить тренированный иммунитет. В одном исследовании Риксен и его коллеги провели 16-недельную программу, в рамках которой людям в возрасте 55 лет и старше предлагалось увеличить физическую активность. Когда по окончании программы они проверили моноциты участников в лаборатории, то обнаружили, что клетки вырабатывали меньшее количество цитокинов, чем раньше. Однако исследование было небольшим - всего 16 человек, и специалисты все еще проверяют, повлияли ли вмешательства на эпигенетические изменения или другие признаки тренированного иммунитета.
Независимо от того, является ли цель профилактикой или устранением последствий, тренированный иммунитет позволяет применять новые подходы. "Я думаю, что открыто целое поле для изучения лекарственных препаратов, чтобы по-настоящему заняться этой перспективой тренированного иммунитета при атеросклерозе", - говорит Лютгенс.
Прогноз на будущее состоит в том, что эта ветвь иммунной системы может быть избавлена от своих потенциально вредных эффектов без потери всех преимуществ, которые она приносит.