Каждый день ваша поджелудочная железа вырабатывает около одной чашки пищеварительных соков - смеси молекул, способных расщеплять пищу, которую вы едите.
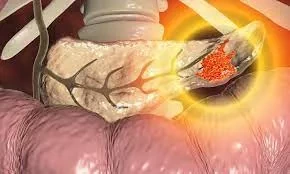
Но если эти мощные молекулы активируются до того, как они попадут в кишечник, они могут повредить саму поджелудочную железу - переварить те самые клетки, которые их создали, привести к болезненному воспалению, известному как панкреатит, и предрасположить человека к раку поджелудочной железы.
Как сообщают ученые в журнале Gastroenterology, белок, известный как гамма-рецептор, связанный с эстрогеном (ERR ɣ), имеет решающее значение для предотвращения самопереваривания поджелудочной железы. Более того, они обнаружили, что у людей с панкреатитом уровень ERR ɣ в клетках, пораженных этим воспалением, ниже. Эти результаты позволяют предположить, что новые методы лечения, направленные на регулирование активности ERR ɣ, могут помочь предотвратить или вылечить панкреатит и рак поджелудочной железы.
"Наши результаты дают новое представление как о базовой биологии функционирования клеток поджелудочной железы, так и о том, что может быть причиной панкреатита и рака поджелудочной железы", - говорит соавтор работы профессор Рональд Эванс.
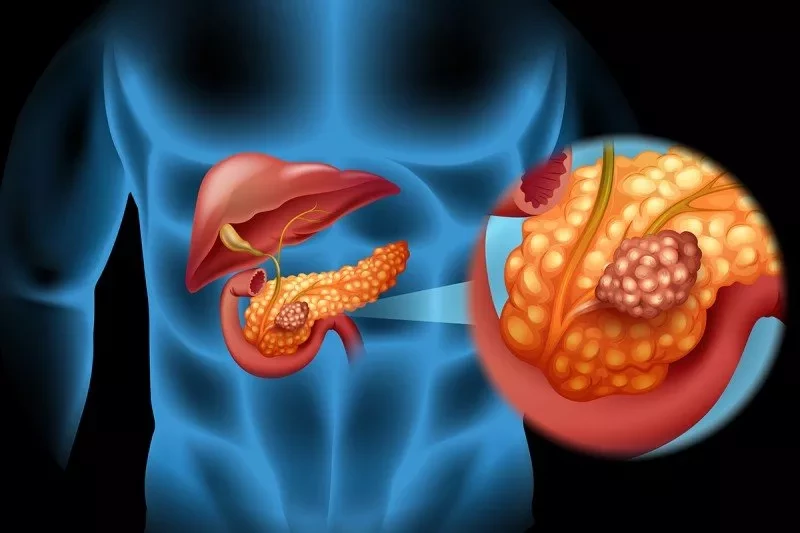
Поджелудочная железа является домом для двух основных типов клеток с различными функциями: бета-клеток, выделяющих инсулин для контроля уровня сахара в крови, и ацинарных клеток, вырабатывающих пищеварительные соки. Эванс и его коллеги ранее обнаружили, что ERR ɣ помогает бета-клеткам поджелудочной железы выделять инсулин и может быть полезен для лечения диабета. В ходе последующих исследований группа также обнаружила, что у мышей, лишенных ERR ɣ, развивается тяжелый панкреатит.
Чтобы понять роль ERR ɣ в ацинарных клетках поджелудочной железы, исследователи сравнили мышей, а также изолированные клетки с белком и без него. Они обнаружили, что ERR ɣ необходим для функционирования митохондрий ацинарных клеток - органелл, вырабатывающих энергию.
"С 1960-х годов известно, что митохондрии являются основным источником энергии в ацинарных клетках, но фактор, который контролирует эту жизненно важную программу производства энергии в ацинарных клетках, долгое время оставался загадкой", - рассказывает Эванс. Без ERR ɣ ацинарные клетки не только имеют дисрегуляцию энергетических функций, но и, как следствие, неправильно активируют пищеварительные ферменты для запуска процесса самопереваривания.
"Митохондрии в этих клетках должны быть особенно прочными", - говорит Эванс. "Если что-то идет не так, активируются пищеварительные ферменты, и начинается процесс самопереваривания поджелудочной железы". Группа показала, что в отсутствие ERR ɣ начинается не только самопереваривание ацинарных клеток поджелудочной железы, но и клеточные изменения, указывающие на раннюю стадию рака поджелудочной железы.
Затем исследователи обратились к данным пациентов с панкреатитом, чтобы определить, насколько результаты, полученные на мышах и в лаборатории, соответствуют заболеванию человека. Они сравнили биопсии при панкреатите с биопсиями, взятыми из нормальных клеток поджелудочной железы, включая здоровые участки поджелудочной железы у тех же пациентов. Клетки, пораженные панкреатитом, как они обнаружили, имели более низкий уровень ERR ɣ.
"Мы изучили данные по разным регионам и группам пациентов и обнаружили, что уровень ERR ɣ очень последовательно снижается при панкреатите", - отмечает Эванс.
Далее Эванс и его коллеги показали, что уровни 83 других генов, многие из которых напрямую регулируются ERR ɣ, также были изменены в образцах панкреатита. Более того, когда они изучили данные двух крупных исследований, сравнивающих экспрессию генов у людей, они обнаружили, что некоторые из этих 83 генов связаны с редкими типами наследственного панкреатита и рака поджелудочной железы. "Тот факт, что это было связано с пациентами с хроническим панкреатитом, говорит о том, что ERR ɣ имеет клиническое значение и в будущем может стать хорошей мишенью для лекарственных препаратов", - утверждает Эванс.
Исследователи планируют дальнейшие исследования для углубленного изучения предраковых изменений, к которым приводит дисрегуляция ERR ɣ и панкреатит, а также того, как лекарства могут помочь увеличить ERR ɣ для профилактики или лечения заболеваний поджелудочной железы.
Jinhyuk Choi et al. Эстроген-регулируемый рецептор γ поддерживает функцию и идентичность ацинарных клеток поджелудочной железы, регулируя клеточный метаболизм (аннотация).
Митохондриальная дисфункция нарушает синтез и секрецию пищеварительных ферментов в ацинарных клетках поджелудочной железы и играет основную роль в этиологии экзокринных заболеваний поджелудочной железы. Однако транскрипционные механизмы, регулирующие функцию митохондрий для поддержания физиологии ацинарных клеток, мало изучены. В данном исследовании мы стремились выяснить функцию рецептора γ, связанного с эстрогеном (ERRγ), в митохондриальном гомеостазе и производстве энергии ацинарных клеток поджелудочной железы.
Методы
Для изучения функции ERRγ в экзокринной поджелудочной железе были созданы две модели ингибирования ERRγ: мыши дикого типа, обработанные GSK5182, и мыши с условным нокаутом ERRγ (cKO). Чтобы определить функциональную роль ERRγ в ацинарных клетках поджелудочной железы, мы провели гистологический и транскриптомный анализ поджелудочной железы, полученной от мышей ERRγ cKO. Чтобы определить значимость этих результатов для заболеваний человека, мы проанализировали транскриптомные данные из нескольких независимых человеческих когорт и провели исследования генетической ассоциации для вариантов ESRRG в двух различных когортах людей с панкреатитом.
Результаты
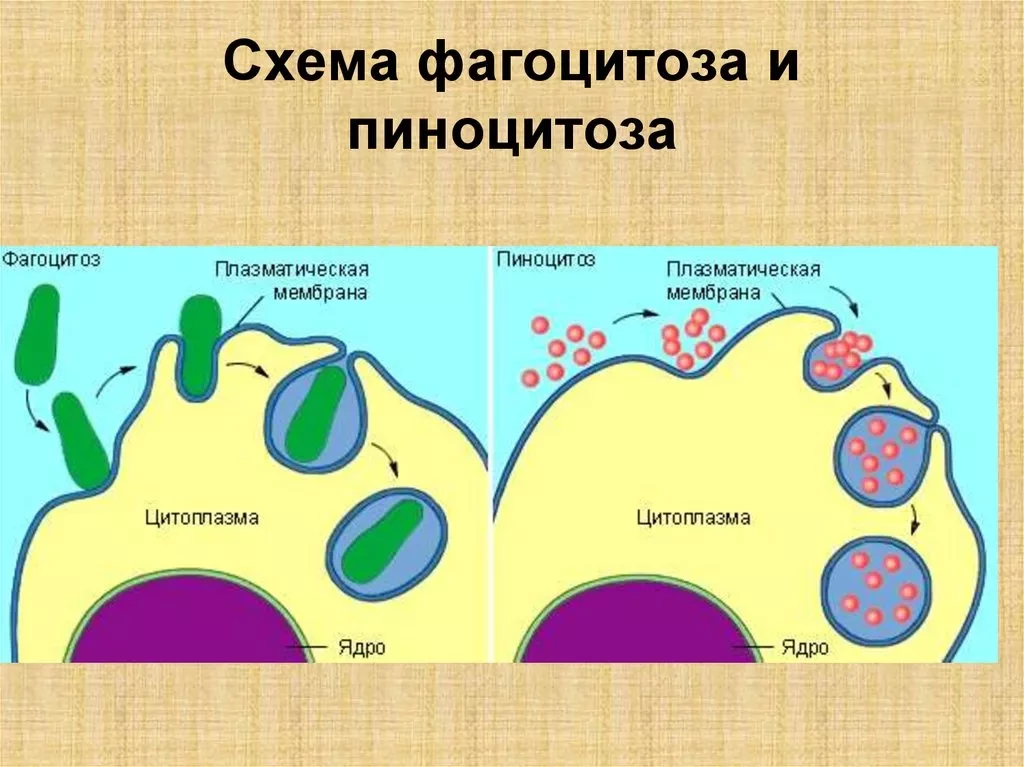
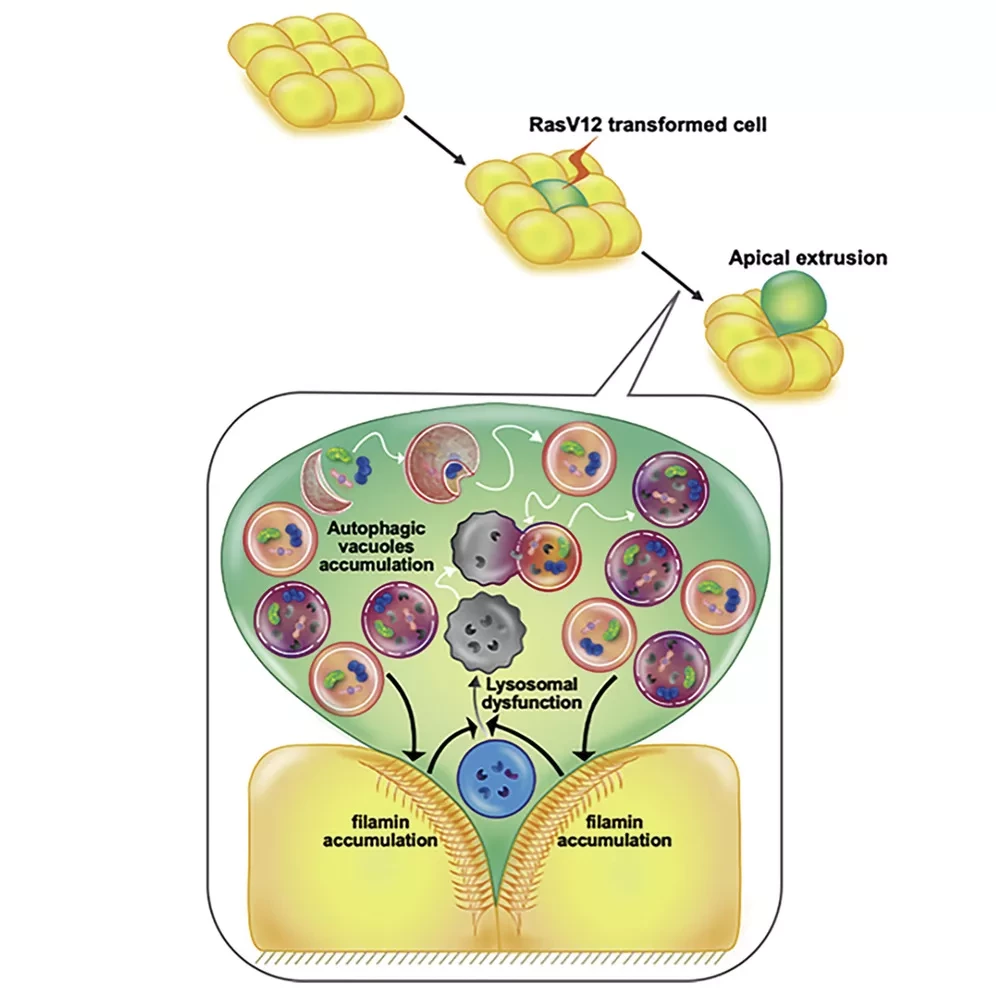
Блокирование функции ERRγ у мышей путем генетической делеции или лечения обратным агонистом приводит к поразительным панкреатитоподобным фенотипам, сопровождающимся воспалением, фиброзом и гибелью клеток. Механистически, потеря ERRγ в первичных ацинусах отменяет экспрессию мессенджерной РНК и уровни белка генов митохондриального комплекса окислительного фосфорилирования, что приводит к дефекту энергетики ацинарных клеток. Митохондриальная дисфункция, вызванная делецией ERRγ, в дальнейшем вызывает дисфункцию аутофагии, стресс эндоплазматического ретикулума и выработку реактивных форм кислорода, что в конечном итоге приводит к гибели клеток.
Интересно, что ацинарные клетки с дефицитом ERRγ, избежавшие гибели клеток, приобретают характеристики протоковых клеток, что указывает на роль ERRγ в метаплазии ацинаров в протоки. В соответствии с нашими результатами, полученными на мышах с сКО ERRγ, экспрессия ERRγ была значительно снижена у пациентов с хроническим панкреатитом по сравнению с нормальными людьми. Кроме того, исследования генетической ассоциации в области локуса-кандидата выявили множество однонуклеотидных вариантов ERRγ, которые связаны с хроническим панкреатитом.
Выводы
В совокупности наши результаты свидетельствуют о важной роли ERRγ в поддержании транскрипционной программы, которая поддерживает митохондриальную функцию ацинарных клеток и органеллярный гомеостаз, и обеспечивают новую молекулярную связь между ERRγ и экзокринными заболеваниями поджелудочной железы.