Недавно охарактеризованный белок может стать недостающим звеном для объяснения редкого метаболического заболевания и одновременно предложить новое понимание таких распространенных расстройств, как ожирение и диабет 2 типа.
Ученые давно пытались выяснить, почему симптомы некоторых заболеваний могут ограничиваться только одной тканью, в то время как они вызваны единственным дефектным белком, присутствующим во всем организме.
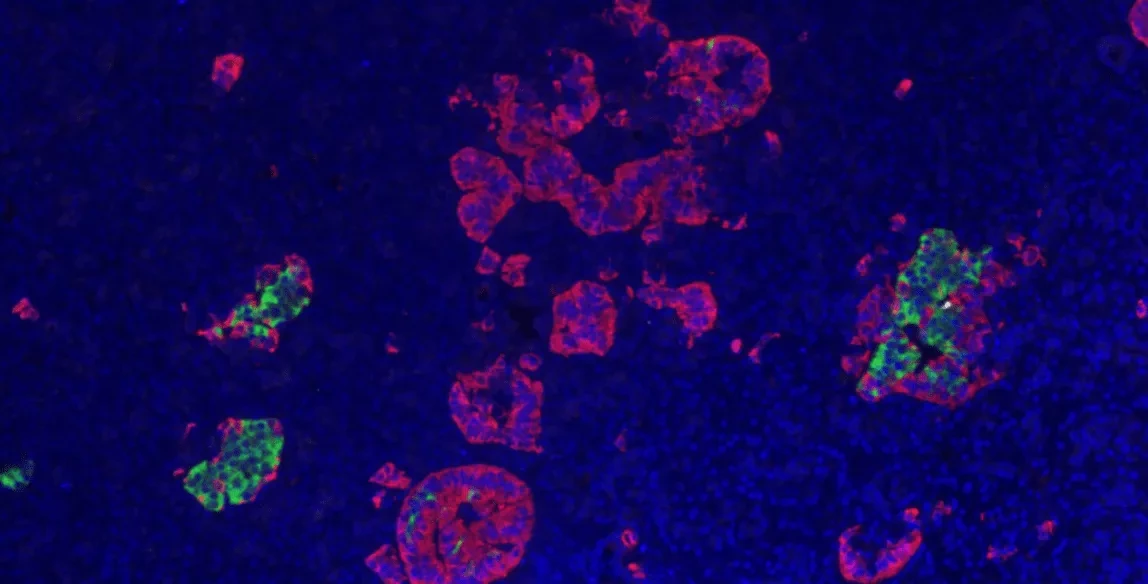
Семейная частичная липодистрофия типа 2 (FPLD2) - редкое заболевание, вызывающее диабет, потерю жировой ткани на руках и ногах и чрезмерное развитие мышц, но при этом дефектный белок, ламин А, содержится во всех клетках. Ученые Эдинбургского университета обнаружили, что у мышей, лишенных белка Tmem120a, который в основном содержится в жировых клетках, наблюдаются симптомы, схожие с FPLD2.
Tmem120a принадлежит к группе белков, известных как NETs, которые помогают обеспечить правильную организацию и считывание генетического материала клетки, находящегося в командном центре клетки - ядре. Они обнаружили, что Tmem120a играет ключевую роль в нормальном развитии жировой ткани и здоровом метаболизме, способствуя экспрессии генов жировой ткани и выключая гены мышечной ткани в жировой ткани. Эти эффекты, по-видимому, обусловлены способностью Tmem120a высвобождать части генома, контролирующие жировой обмен, одновременно привлекая мышечные гены.
Когда гены находятся на периферии ядра, они, как правило, выключены, и ученые обнаружили, что неправильное расположение генов у мышей, лишенных Tmem120a, также происходит у пациентов с FPLD2. Авторы исследования, опубликованного в Nature Communications, предполагают, что поскольку Tmem120a обнаруживается в основном в жировой ткани, он опосредует жироспецифичность дефекта, вызванного дефектным белком ламин А, ранее связанным с FPLD2.
Исследования генетических дефектов, вызывающих метаболические заболевания, показывают, что они носят комплексный характер с участием многих генов; таким образом, Tmem120a, влияя на расположение многих генов, также может быть вовлечен в этот процесс. Полученные результаты могут иметь более широкое значение для других метаболических заболеваний, таких как диабет, инсулинорезистентность, непереносимость глюкозы и ожирение, а также для мышечных расстройств и телосложения.
Симптомы проявились только у мышей, которых кормили высококалорийной диетой, что соответствует симптомам FPLD2, которые часто проявляются позже в жизни и требуют тщательно контролируемой диеты. Этот механизм может объяснить, почему некоторые заболевания, такие как диабет, проявляются только при нагрузке на организм - например, при высококалорийной диете, которой кормили мышей, лишенных гена Tmem120a.
Функциональные дефекты других белков NET связаны со многими заболеваниями человека, такими как мышечная дистрофия, кардиомиопатия, заболевания крови и костей, рак и синдромы преждевременного старения. Другие сложные заболевания могут иметь схожий механизм, при котором NET, влияющие на расположение генов, вызывают небольшие изменения в экспрессии множества генов, так что механизмы продолжают функционировать, но с пониженной эффективностью, что приводит к появлению симптомов только при определенных обстоятельствах.
Рафал Чапиевски, первый автор статьи, говорит:
"Наиболее интересным для меня является открытие нового механизма роста мышц, наблюдаемого при липодистрофии, что открывает новые потенциальные возможности для увеличения мышечной массы, которая теряется, например, у астронавтов во время космических путешествий, при мышечной дистрофии или при потере мышц в результате травм".
Czapiewski, R. et al. Неправильное расположение геномных локусов у нокаутных мышей Tmem120a приводит к латентной липодистрофии (аннотация).
О том, как формируется наблюдаемый специфический для жировой ткани паттерн трехмерно-пространственной организации генома, известно мало. В данном отчете мы сообщаем, что специфический для адипоцитов нокаут гена, кодирующего трансмембранный белок ядерной оболочки Tmem120a, нарушает организацию жирового генома, вызывая синдром липодистрофии. Дефицит Tmem120a широко подавляет экспрессию генов пути липидного метаболизма и индуцирует экспрессию миогенных генов путем перемещения генов, энхансеров и локусов, кодирующих миРНК, между ядерной периферией и внутренним сектором.
Мыши Tmem120a-/-, особенно самки, демонстрируют синдром липодистрофии, схожий с человеческой семейной частичной липодистрофией FPLD2, с выраженной инсулинорезистентностью и метаболическими дефектами, которые проявляются при воздействии жирной диеты. Интересно, что аналогичные дефекты организации генома наблюдались в клетках пациентов с FPLD2, которые несут мутации белка ядерной оболочки, кодирующего LMNA.
Наши данные показывают, что функции организации генома TMEM120A влияют на многие функции жировой ткани, и его потеря может приводить к расстройствам спектра жировой ткани, включая механизм, основанный на миРНК, который может объяснить гипертрофию мышц при липодистрофии человека.