Валидирование генетической диагностики неврологических и нервно-мышечных заболеваний с помощью более быстрых, компактных и дешевых технологий секвенирования.
Новый ДНК-тест, разработанный исследователями из Института медицинских исследований Гарвана в Сиднее, позволяет быстрее и точнее выявить ряд труднодиагностируемых неврологических и нервно-мышечных генетических заболеваний, чем существующие тесты.
"Мы правильно диагностировали у всех пациентов уже известные заболевания, включая болезнь Хантингтона, синдром ломкой Х-хромосомы (синдром Мартина-Белл), наследственную мозжечковую атаксию, миотоническую дистрофию, миоклоническую эпилепсию, болезнь двигательных нейронов и другие", - говорит Айра Девесон, старший автор исследования. Заболевания, на которые направлен тест, относятся к категории более 50 заболеваний, вызванных необычно длинными повторяющимися последовательностями ДНК в генах человека, известных как "болезни экспансии тринуклеотидных повторов" (STR или БЭТП). Их часто трудно диагностировать из-за сложных симптомов, которые проявляются у пациентов, сложной природы этих повторяющихся последовательностей и ограничений существующих методов генетического тестирования", - говорит Девесон.
Исследование, опубликованное в журнале Science Advances, показывает, что тест является точным, и позволяет исследователям начать валидацию, чтобы сделать тест доступным в лабораториях по всему миру.
Один из пациентов, участвовавших в исследовании, Джон, впервые понял, что что-то не так, когда у него возникли необычные проблемы с равновесием во время катания на лыжах. "Меня очень беспокоили симптомы, которые с годами становились все более серьезными: от активного и подвижного человека до неспособного ходить без поддержки. Я проходил тест за тестом в течение более десяти лет и не получал абсолютно никаких ответов на вопрос, в чем дело", - говорит Джон, которому в конце концов поставили диагноз редкого генетического заболевания CANVAS, поражающего мозг. "Было очень приятно наконец-то подтвердить мой диагноз генетически, и радостно осознавать, что в ближайшем будущем другие люди с подобными заболеваниями смогут узнать диагноз быстрее, чем я", - говорит он.
"Для таких пациентов, как Джон, новый тест станет переломным моментом, помогая покончить с тем, что часто может быть тяжелой диагностической одиссеей", - считает Девесон. "Расстройства БЭТП могут передаваться по наследству, могут быть опасны для жизни и обычно влекут за собой повреждение мышц и нервов, а также другие осложнения".
По словам Девенсона, в настоящее время генетическое тестирование на наличие БЭТП может быть "точным и безошибочным". Когда у пациентов появляются симптомы, бывает трудно определить, какая из этих 50 с лишним генетических экспансий у них может быть, поэтому врач должен решить, на какие гены проводить тестирование, основываясь на симптомах и семейной истории. Если тест дает отрицательный результат, пациент остается без ответов. Такое тестирование может продолжаться годами, так и не найдя генов, связанных с заболеванием. Мы называем это "диагностической одиссеей", и это может быть довольно стрессовым для пациентов и их семей", - говорит он.
"Новый тест полностью изменит наши методы диагностики этих заболеваний, поскольку теперь мы можем проверить все нарушения сразу с помощью одного теста ДНК и поставить четкий генетический диагноз, помогая пациентам избежать многих лет ненужных биопсий мышц или нервов для выявления заболеваний, которых у них нет, или рискованного лечения, подавляющего их иммунную систему."
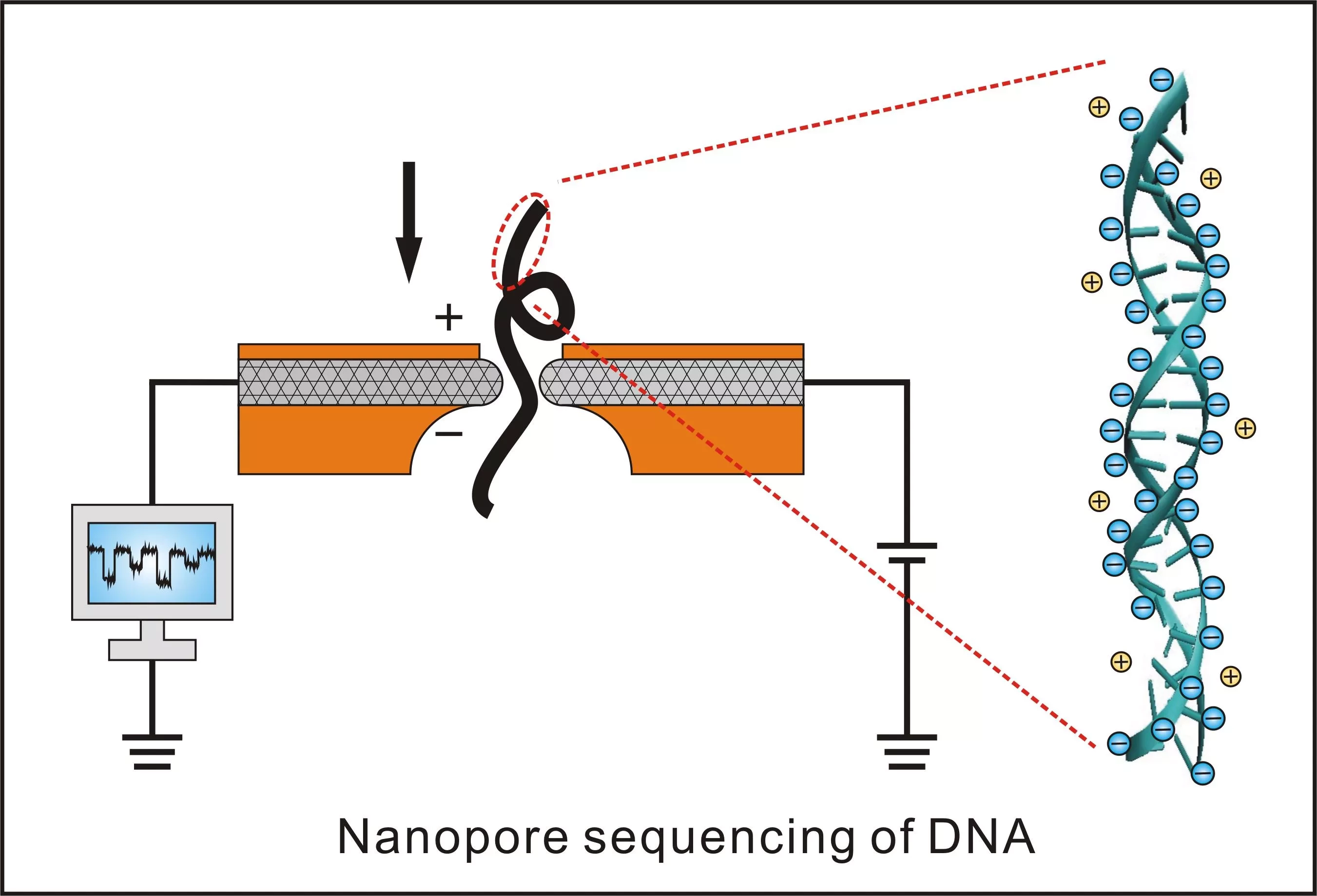
Хотя расстройства БЭТП нельзя вылечить, более быстрая диагностика может помочь врачам раньше выявить и вылечить осложнения болезни, например, проблемы с сердцем, характерные для атаксии Фридрейха. Используя один образец ДНК, обычно полученный из крови, тест работает путем сканирования генома пациента с помощью технологии, называемой нанопоровым секвенированием.
"Мы запрограммировали устройство Nanopore так, чтобы оно нацеливалось примерно на 40 генов, которые, как известно, вовлечены в эти расстройства, и считывало длинные, повторяющиеся последовательности ДНК, которые вызывают заболевание", - говорит Девенсон. "Распутывая две нити ДНК и считывая повторяющиеся буквенные последовательности (комбинации A, T, G или C), мы можем сканировать гены пациента на наличие аномально длинных повторов, которые являются признаками заболевания. В одном тесте мы можем найти все известные сиквенсы, вызывающие заболевания, и потенциально обнаружить новые сиквенсы, которые могут быть вовлечены в еще не описанные заболевания."
"Нанопоровая технология, используемая в тесте, меньше и дешевле, чем стандартные тесты, что, как надеется группа, облегчит ее внедрение в лаборатории. "Благодаря технологии нанопорового секвенирования генов устройство уменьшилось с размеров холодильника до размеров степлера и стоит около 1000 долларов, по сравнению с сотнями тысяч, необходимых для обычных технологий секвенирования ДНК", - рассказывает Девесон.
Специалисты ожидают, что их новая технология будет использоваться в диагностической практике в течение следующих двух-пяти лет. Одним из ключевых шагов на пути к этой цели является получение соответствующей клинической аккредитации метода. По словам Джины Равенскрофт, соавтора исследования и исследователя, занимающегося генетикой редких заболеваний в Институте медицинских исследований имени Гарри Перкинса, после аккредитации тест также изменит исследования генетических заболеваний.
"Генетические заболевания, возникающие во взрослом возрасте, не привлекают такого внимания исследователей, как те, которые проявляются в раннем возрасте", - говорит она. "Найдя больше людей с этими редкими заболеваниями, развивающимися у взрослых, а также тех, кто может быть предсимптоматическим, мы сможем больше узнать о целом ряде редких заболеваний с помощью когортных исследований, что в противном случае было бы трудно сделать".
Igor Stevanovski et al. Комплексная генетическая диагностика заболеваний с экспансией тандемных повторов с помощью программируемого целевого нанопорового секвенирования (аннотация).
Более 50 неврологических и нервно-мышечных заболеваний вызываются экспансиями коротких тандемных повторов (STR), причем на сегодняшний день выявлено 37 различных генов. Мы описываем использование программируемого направленного секвенирования с функцией ReadUntil от Oxford Nanopore для параллельного генотипирования всех известных невропатогенных STR в одном тесте. Наш подход обеспечивает точную сборку гаплотипов и профилирование метилирования ДНК участков STR из списка заранее определенных кандидатов. Это позволило правильно диагностировать всех людей в небольшой когорте (n = 37), включая пациентов с различными нейрогенетическими заболеваниями (n = 25).
Целенаправленное секвенирование решает проблемы больших и сложных расширений STR, которые затрудняют стандартные молекулярные тесты и секвенирование с коротким прочтением, и выявляет неканонические конформации STR-мотивов и прерывания внутренних сиквенсов. Мы наблюдали разнообразие STR-аллелей известной и неизвестной патогенности, что позволяет предположить, что секвенирование с длинным прочтением изменит генетический ландшафт нарушений, связанных с повторными заболеваниями. Наконец, мы показали, как включение фармакогеномных генов в качестве вторичных мишеней ReadUntil может помочь в лечении пациентов.