Новый метод позволяет выявить идентичность и активность клеток в органе или опухоли с беспрецедентным разрешением, говорится в исследовании, проведенном под руководством ученых из Weill Cornell Medicine и Нью-Йоркского геномного центра.
Метод, описанный 2 января в статье в журнале Nature Biotechnology, позволяет регистрировать активность генов и наличие ключевых белков в клетках в образцах тканей, сохраняя при этом информацию о точном местоположении клеток. Это позволяет создавать сложные, богатые данными "карты" органов, включая больные органы и опухоли, что может быть востребовано в фундаментальных и клинических исследованиях. "Эта технология очень интересна, потому что она позволяет нам составить карту пространственной организации тканей, включая типы клеток, их активность и межклеточные взаимодействия, чего никогда не было раньше", - рассказывает соавтор исследования Дэн Ландау.
Новый метод является частью масштабных усилий ученых и инженеров по разработке лучших способов "увидеть" в микромасштабе, как работают органы и ткани. В последние годы исследователи добились больших успехов, в частности, в технике профилирования активности генов и других уровней информации в отдельных клетках или небольших группах клеток. Однако эти методы, как правило, требуют лизирования тканей и отделения клеток от их соседей, поэтому информация о первоначальном расположении профилируемых клеток в тканях теряется. Новый метод позволяет получить и пространственную информацию, причем с высоким разрешением.
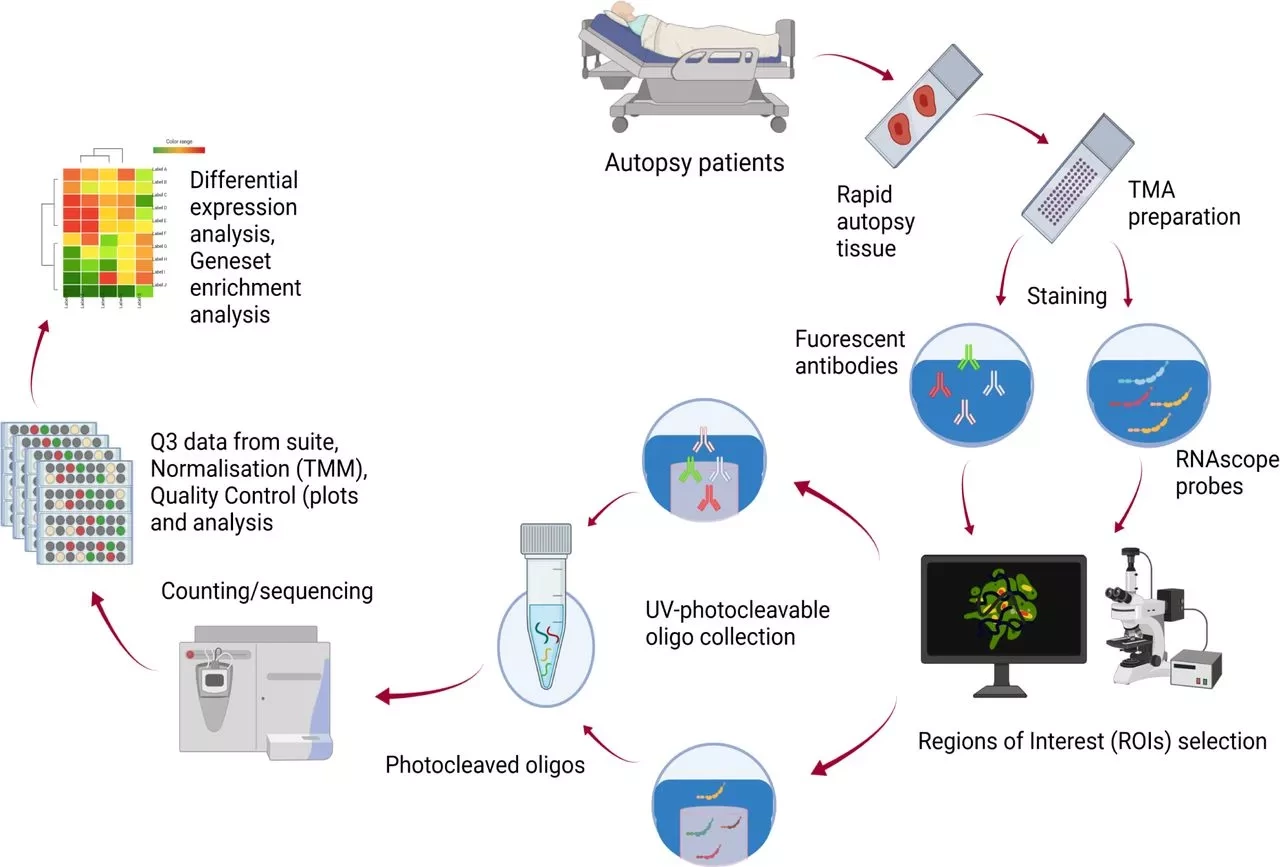
Метод, получивший название Spatial PrOtein and Transcriptome Sequencing (SPOTS), частично основан на существующей технологии компании 10x Genomics. В нем используются стеклянные предметные стекла, которые подходят для визуализации образцов тканей с помощью обычных патологоанатомических микроскопов, но при этом они покрыты тысячами специальных молекул-зондов. Каждая из молекул зондов содержит молекулярный "штрих-код", обозначающий ее двумерное положение на предметном стекле. Когда тонко нарезанный образец ткани помещают на предметное стекло и делают его клетки проницаемыми, молекулы зонда на предметном стекле захватывают мессенджерные РНК (мРНК) соседних клеток, которые, по сути, являются транскриптами активных генов.
Метод включает использование дизайнерских антител, которые связываются с интересующими белками в ткани, а также связываются со специальными молекулами-зондами. С помощью быстрых автоматизированных методов исследователи могут идентифицировать захваченные мРНК и выбранные белки и нанести их на карту в точном соответствии с их первоначальным расположением в образце ткани. Полученные карты можно рассматривать отдельно или сравнивать со стандартным патологоанатомическим изображением образца.
Исследователи продемонстрировали SPOTS на ткани нормальной селезенки мыши, выявив сложную функциональную архитектуру этого органа, включая скопления различных типов клеток, их функциональные состояния и то, как эти состояния меняются в зависимости от расположения клеток.
Чтобы продемонстрировать потенциал SPOTS в исследовании рака, авторы также использовали его для составления карты клеточной организации опухоли молочных желез у мышей. На полученной карте макрофаги, находились в двух различных состояниях, обозначаемых белковыми маркерами: одно состояние было активным и боролось с опухолью, другое - иммуносупрессивным и формировало барьер для защиты опухоли. "Мы видим, что эти две подгруппы макрофагов находятся в разных областях опухоли и взаимодействуют с разными клетками - и это различие в микроокружении, вероятно, определяет их различные состояния активности", - пояснил Ландау.
Такие детали иммунной среды опухоли - детали, которые часто не удается выяснить из-за малочисленности иммунных клеток в опухоли - могут помочь объяснить, почему некоторые пациенты отвечают на иммуноукрепляющую терапию, а некоторые нет, и таким образом могут помочь в разработке будущих иммунотерапий, добавил он.
Начальная версия SPOTS имеет такое пространственное разрешение, что каждый "пиксель" полученного набора данных суммирует информацию о генной активности по крайней мере нескольких клеток. Однако исследователи надеются вскоре сузить это разрешение до отдельных клеток, добавив при этом другие слои ключевой клеточной информации, сообщил Ландау.
Nir Ben-Chetrit et al. Интеграция пространственного профилирования всего транскриптома с белковыми маркерами (аннотация).
Пространственная транскриптомика и протеомика предоставляют взаимодополняющую информацию, которая независимо друг от друга изменила наше понимание сложных биологических процессов. Однако экспериментальная интеграция этих методов ограничена.
Чтобы преодолеть это, мы разработали Spatial PrOtein and Transcriptome Sequencing (SPOTS) для высокопроизводительной одновременной пространственной транскриптомики и профилирования белков. По сравнению с унимодальными измерениями, SPOTS значительно улучшает разрешение сигнала и кластеризацию клеток, а также увеличивает возможности обнаружения при анализе дифференциальной экспрессии генов в различных регионах ткани.