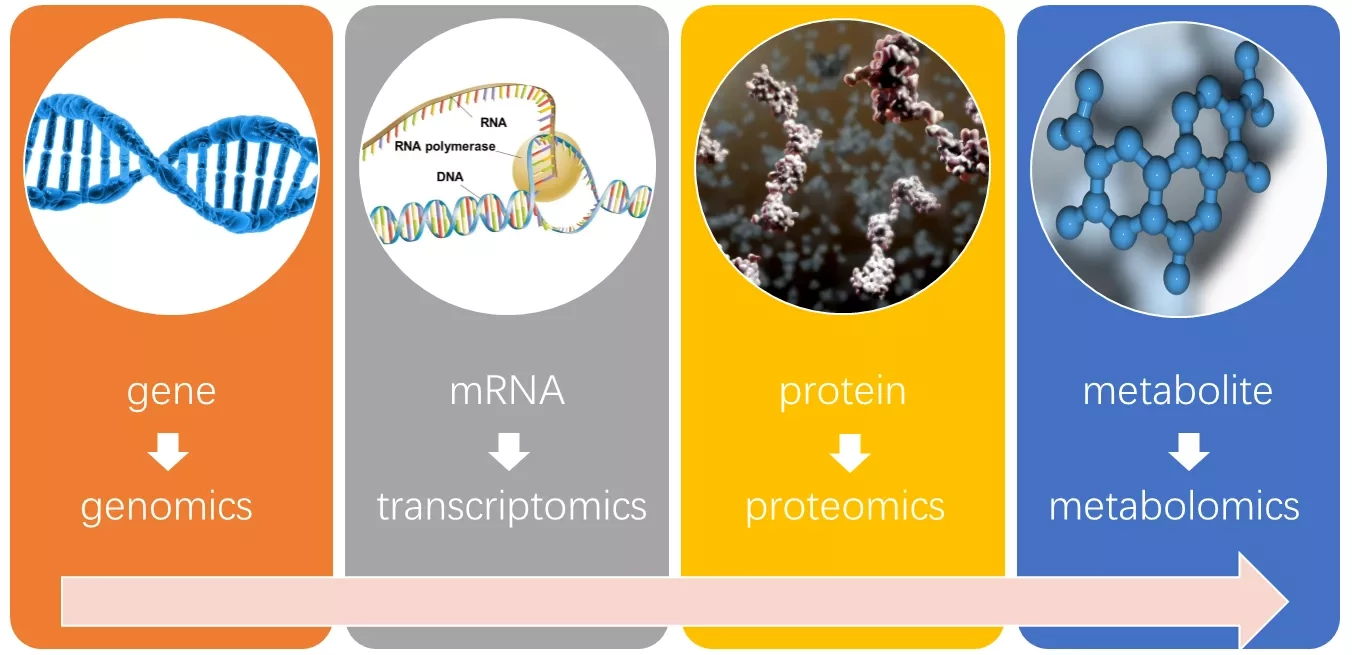
В недавнем исследовании, опубликованном в журнале Nature Medicine, ученые систематически проводили генетический анализ почти 20 000 женщин и мужчин с точки зрения >900 метаболитов.
Метаболиты, циркулирующие в организме человека, отражают физиологию человека и его химическую индивидуальность. Метаболизм человека нарушается при ряде заболеваний и зависит от множества диетических, генетических, лекарственных и связанных с заболеваниями факторов. Существует широкий спектр высокопроизводительных биомедицинских технологий, позволяющих оценить генетические факторы, влияющие на физиологию человека, однако данные о корегуляции различных метаболитов ограничены. В настоящем исследовании ученые изучили генетические детерминанты вариаций в физиологии человека с использованием нецелевых метаболомных данных.
Группа проанализировала генетическую архитектуру 913 метаболитов у >14 000 человек. Данные были использованы для определения генетически влияющих метаботипов (GIMs) или групп метаболитов, на которые влияет генетический сигнал ≥1,0. Были использованы образцы из двух когортных исследований, проводившихся в Великобритании: INTERVAL и EPIC-Norfolk, и затем был проведен анализ. Метаболиты были измерены с помощью жидкостной хроматографии и масс-спектрометрии и классифицированы как относящиеся к липидному, аминокислотному, ксенобиотическому, нуклеотидному, пептидному, углеводному, кофакторному, витаминному и энергетическому обмену.
Соединения с неопределенной химической идентичностью были названы неаннотированными соединениями. Для анализа проводилось многомерное линейное регрессионное моделирование. Метаболомные измерения проводились в период с 2015 по 2017 год для образцов EPIC-Norfolk. Уровни метаболитов оценивались в двух сериях примерно по 6 000 образцов в каждой. Команда подтвердила ассоциации вариантов и метаболитов путем мета-анализа совокупности обнаружения и валидации данных.
Среди участников исследования EPIC-Norfolk 5 698 и 5 841 человек были отнесены к группам валидации и обнаружения, соответственно. Были проведены анализы генотипирования и интерполяции, в ходе которых группа вычислила генетически предсказанные уровни метаболитов ("показатели метаболитов") у участников UK Biobank с использованием взвешенных генетических показателей и оценила их ассоциации с 1 457 сопоставленными терминами заболеваний ("фекодами"). Анализ геномных ассоциаций (GWAS) проводился для каждого метаболита отдельно для всех образцов. Далее были проведены условный анализ, анализ колокализации и анализ обогащения для генов, вызывающих врожденные ошибки метаболизма (IEM).
Была оценена аллельная гетерогенность, а также генетическая корегуляция различных метаболитов. Группа также провела фенотипический анализ генетических вариантов, связанных с метаболитами, и определила метаболические ассоциации. Полученные результаты были технически подтверждены с использованием данных полной экзомной последовательности (WES) из 3 924 образцов исследования INTERVAL.
Были определены наиболее вероятные причинные гены, а новизна ассоциации вариантов была оценена на основе сравнения полученных результатов с результатами двух ранее проведенных исследований. На основе выявленных генетических ассоциаций и вручную проанализированной научной литературы были определены высокодостоверные причинные гены, регулирующие метаболиты, и проведена оценка их клинической значимости по >1 400 фенотипам.
Наблюдалось сходство фенотипических и метаболических проявлений редких генов, вызывающих IEM, с генетическими вариантами генов, выявленными в общей популяции. Всего было выявлено 423 GIMs, включая в основном ≤15 генетических вариантов и ≤89 метаболитов. Для 62% (n=264) GIMs был определен ген из 253 вероятных причинных генов на основе обширного анализа данных. Такие GIM, как стероидная 5α-редуктаза 2 (SRD5A2) и дигидропиримидиндегидрогеназа (DPYD), показали важное клиническое значение.
Более высокая активность SRD5A2 была связана с большим риском облысения у мужчин. Генетические ассоциации соответствовали меньшей активности SRD5A2 и меньшим уровням андростерона, эпиандростерона, 3α-андростандиола и конъюгатов 3β-андростандиола. Были обнаружены общие генетические сигналы между различными метаболитами андрогенов и облысением по мужскому типу, причем rs112881196 является причинным вариантом. Локус десатуразы жирных кислот (FAD)S1/S2 был связан с большинством аннотированных метаболитов.
Средняя фенотипическая дисперсия, объясненная условно независимыми вариантами, составила 5,2%, причем наибольшая для классов аминокислот и энергетических веществ. Более низкие уровни ингибитора SRD5A были связаны с более значительным риском депрессии, при этом rs62142080 был вероятным причинным вариантом. Вариант rs72977723 связан с расщеплением урацила, в то время как rs184097503 и rs28933981 повышают способность к переносу тироксина. Наблюдались GIMs, отражающие многочисленные функции генов, например, транспортеров SLC7A2 (Slc7a2 solute carrier family 7), связанных с уровнем аргинина или лизина.
Наблюдалось 8,0-кратное обогащение генов, вызывающих IEM, причем варианты IEM были сопоставлены с генами, вызывающими нарушения, связанные с митохондриями, аминокислотами и жирными кислотами. Более низкие уровни ванилилманделата были связаны с более низким риском развития гипертонии, причем rs6271 был причинным вариантом. Также были выявлены гены, вызывающие ишемическую болезнь сердца [PCSK9 (Proprotein convertase subtilisin/kexin type 9), SORT1 (Sortiliin 1) и LDLR (low-density lipoprotein receptor)], макулярная дегенерация [LIPC (печеночная липаза) и аполипопротеин Е (APOE)/аполипопротеин С (APOC) 1,2,4], болезнь Крона [GCKR (регулятор глюкокиназы) и FADS2] и хроническая болезнь почек [GATM (глицин-амидинотрансфераза)].
Наблюдалась связь между метаболитами и заболеваниями, такими как уровень уратов при подагре [отношение шансов (ОР) 2,2], желчных кислот при желчнокаменной болезни (ОР 0,6 для гликохиохолата) и сложных липидов при гиперхолестеринемии [ОР 1,8 для 1-дигомо-линолеоил-ГПК (20:2)]. Было установлено, что гомоаргинин плазмы играет ключевую роль в патологии хронической болезни почек, а 3-метилглутарилкарнитин защищает от развития доброкачественных новообразований в толстой кишке.
В целом, результаты исследования позволили выявить генетические детерминанты вариаций метаболитов человека и могут послужить руководством для будущих ассоциативных оценок метаболома.
Surendran, P., Stewart, I.D., Au Yeung, V.P.W. et al. Редкие и общие генетические детерминанты метаболической индивидуальности и их влияние на здоровье человека (аннотация).
Концепция Гаррода о "химической индивидуальности" способствовала пониманию молекулярных истоков человеческих заболеваний. Нецелевые высокопроизводительные метаболомные технологии позволяют получить углубленный "снимок" метаболизма человека.
Мы изучили генетическую архитектуру метаболома плазмы крови человека с помощью 913 метаболитов, определенных у 19 994 человек, и выявили 2599 ассоциаций между вариантами и метаболитами (P < 1,25 × 10-11) в 330 геномных регионах, причем редкие варианты (частота минорных аллелей ≤ 1%) объясняют 9,4% ассоциаций. Совместно моделируя метаболиты в каждом регионе, мы определили 423 региональных, корегуляторных, вариант-метаболитных кластера, названных генетически воздействующими метаботипами. Мы определили причинные гены для 62,4% этих генетически влияющих метаботипов, что позволило по-новому взглянуть на фундаментальную физиологию метаболитов и их клиническую значимость, включая обнаружение потенциальных неблагоприятных эффектов лекарственных препаратов (DPYD и SRD5A2) с помощью метаболитов. Мы показали сильное обогащение генов, вызывающих врожденные ошибки метаболизма, с примерами ассоциаций метаболитов и клинических фенотипов непатогенных носителей вариантов, соответствующих характеристикам врожденных ошибок метаболизма. Систематическое, фенотипическое наблюдение за генетическими показателями, специфичными для метаболитов, выявило множество потенциальных этиологических связей.